Перевод газовой колонки на сжиженный газ: Инструкция. Перевод газовой колонки Нева 4511 на сжиженный газ
Инструкция. Перевод газовой колонки Нева 4511 на сжиженный газ
Инструкция. Перевод газовой колонки Нева 4511 на сжиженный газ
В газовой колонке Нева 4511 для работы на природном газе установлены жиклеры диаметром 1,28 мм. Этот набор сопел устанавливается в рампу горелки для работы на природном газе с давлением 130 мм. вод. ст. (130 mbar). Рампа у газовой колонки Нева 4511 десятисекционная, т.е. в рампу входят 10 сопел.
Предлагаемый нами комплект сопел для сжиженного газа содержит 10 сопел диаметром 0,75 мм.
Предлагаемый комплект подходит только для данной модели, поскольку, например, у газовой колонки Нева 4510 рампа просто другой конструкции. Тем более что данная модель Невы 4511 нами довольно хорошо изучена. Она проста в монтаже, ремонте и обслуживании. При переводе на сжиженный газ, колонка потребляет порядка киллограмма газа за час работы. Вы сейчас сами убедитесь, что переделка рампы много времени не займет. Для перевода колонки нам понадобиться крестовая отвертка и разводной ключ(38 мм). Саму колонку вовсе не надо демонтировать.
Для перевода колонки нам понадобиться крестовая отвертка и разводной ключ(38 мм). Саму колонку вовсе не надо демонтировать.
Начинаем
Сначала надо отделить рампу. На рампе закреплены электрод розжига (свеча) и датчик наличия (ионизации) пламени. Отделяем их, откручивая два винта.
На фото они обозначены номером №1. После отделения датчика и свечи от рампы, надо вывернуть четыре самореза (№2), которые и закрепляют рампу горелки.
После их отделения берем разводной ключ и откручиваем гайку рампы от газового узла колонки.
Рампа у нас в руках. После того как рампа оказалась у нас в руках, жиклеры лучше всего выворачивать головкой (7 мм), чтобы не повредить шлицы при затягивании новых сопел пассатижами или рожковым ключом (ключик, как и головка на 7 мм). Как видите, для замены сопел от Вашего мозга почти ничего не требуется.
Это все. Удачи Вам!
P.S. Посвящается всем, кто пострадал от некомпетентности продавцов, заказывая газовую колонку Нева 4511 на сжиженном газе, а получил природный. Вы можете просто заказать данный комплект для перевода газовой колонки Нева 4511 на сжиженный газ и перевести колонку сами.
Вы можете просто заказать данный комплект для перевода газовой колонки Нева 4511 на сжиженный газ и перевести колонку сами.
Газовая колонка на сжиженном (баллонном) газе — расход, требования, выбор
Подавляющее большинство выпускаемых проточных и накопительных газовых водонагревателей предназначены для подключения к магистральному газу. Некоторые модели можно переоборудовать под пропан.
Газовая колонка на сжиженном газе имеет несколько отличий. Во время подключения учитывают разницу в характеристиках пропана и метана, отличия во время горения топлива.
Как работает колонка на сжиженном газе
Производители выпускают несколько проточных и накопительных газовых бойлеров, способных работать на пропане. Существуют универсальные модели колонок, которые спокойно функционируют на сжиженном и магистральном газе, после переоборудования и перенастройки.
Отличие водонагревателей на магистральном газе от сжиженного в конструкции горелки. Чтобы понять разницу необходимо представить, как именно происходит сжигание топлива:
- Горит не сам газ, а газовоздушная смесь, которая готовится при прохождении от форсунки до сопла горелки.

- Пропорции метана или пропана и кислорода должны быть строго соблюдены. Богатая на воздух смесь будет плохо гореть, бедная коптить.
- Скорость подачи пропана и метана на горелку разная. Баллонный газ подается под давлением в несколько раз превышающим то, что выдает бытовой магистральный газопровод. Соответственно, чтобы создать нормальные условия для сгорания топлива, необходимо уменьшить скорость подачи пропана, стабилизировать давление, чего добиваются сменой форсунок и установкой редуктора.
Если говорить о технических условиях эксплуатации, то возможность установки проточного или накопительного водонагревателя на сжиженном газе существует в любом частном доме. В отличие от подключения к магистральному газу, нет необходимости в оформлении различных разрешительных документов и изготовления проекта. Бойлер можно подключить к одному или нескольким баллонам, газгольдеру.
Отзывы о колонках на сжиженном газе показывают, что существует рабочий нюанс, который, зачастую, не учитывается при подключении. Заключается он в следующем. Пропан закачивают в баллоны под давлением, за счет чего он становится жидкостью. Газ заполняет емкость приблизительно на ⅔. Жидкость испаряется с поверхности, после чего поступает в редуктор и оттуда подается на горелку водонагревателя.
Заключается он в следующем. Пропан закачивают в баллоны под давлением, за счет чего он становится жидкостью. Газ заполняет емкость приблизительно на ⅔. Жидкость испаряется с поверхности, после чего поступает в редуктор и оттуда подается на горелку водонагревателя.
Сложность заключается в том, что испарение происходит с одновременным отбором тепла. В результате при сильном расходе топлива, наблюдается промерзание стенок баллона. О том, как решить проблему описано в подзаголовке, описывающем нюансы подключения.
Как перевести колонку с метана на пропан
Переоборудование осуществляется заменой некоторых узлов водонагревателя и правильным подключением к газобаллонной установке. Переделка на пропан требует:
- сменить форсунки на основной горелке, в зависимости от модели бойлера их 12-15 шт.;
- если используется полуавтоматическая система розжига, на фитиле заменяют жиклеры.
Таким же способом можно переделать обычную газовую колонку с природного на сжиженный газ. Отличие в том, что в универсальных моделях в заводском комплекте уже находятся форсунки и жиклеры нужного диаметра.
Отличие в том, что в универсальных моделях в заводском комплекте уже находятся форсунки и жиклеры нужного диаметра.
Настройка проточного водонагревателя для работы на сжиженном газе осуществляется с помощью механического блока управления. На корпусе водонагревателя предусмотрены поворотные ручки или рычаги, регулирующие давление газа, подаваемого на горелку. Оптимальным считается режим, при котором языки пламени имеют голубовато-синий цвет.
Какой расход пропана в газовом водонагревателе
Точные затраты указываются в паспорте к бойлеру. К примеру, газовые проточные колонки Bosh, работающие от баллонного газа и имеющие производительность в 25 кВт, в непрерывном режиме расходуют 1 баллон топлива на 50 л в течение 10 часов.
На затраты может влиять тип топлива (зимнее или летнее), его качество. Расход газа в самостоятельно переоборудованных водонагревателях, не предназначенных для сжигания пропана, как правило выше на 5-10%. Отражаются на затратах и ошибки, допущенные при подключении оборудования.
Для удовлетворения потребностей в ГВС 2-3 человек, при условии умеренного использования водонагревателя, расход сжиженного газа составит один 50 л. баллон/мес.
Как выбрать колонку на сжиженном газе
Если планируется приобретение бойлера для подключения к баллонному топливу, лучше сразу приобретать адаптированный к использованию пропана. В инструкции производителя будет указано, что колонка универсальная и может переключаться между природным и сжиженным газом. При выборе также учитывают принцип работы, особенности внутреннего устройства и другие технические и эксплуатационные характеристики.
Принимают во внимание следующие аспекты:
- Принцип нагрева воды — существуют проточные и накопительные нагреватели. У каждой модели есть свои особенности:
- Проточный газовый водонагреватель на сжиженном газе — нагрев осуществляется посредством теплообменника, нагреваемого работающей горелкой, расположенной под змеевиком. Проточная колонка включается при открытии крана ГВС и выключается после его закрытия.

Достоинства: небольшие габариты, относительно невысокая стоимость.
Недостатки: зависимость от давления в подающем трубопроводе ХВС. - Газовый накопительный водонагреватель на сжиженном газе — внутреннее устройство напоминает обычный электрический бойлер, только вместо ТЭНа используется жаровая труба, играющая роль теплообменника. После нагрева вода сохраняется в теплоизолированной емкости. Водонагреватель автоматически поддерживает необходимую температуру нагрева.
Плюсы: емкостный бойлер может работать даже при низком давлении ХВС, потребителю моментально подается горячая вода.
Минусы: высокая стоимость, большие габариты накопительного бака.
- Проточный газовый водонагреватель на сжиженном газе — нагрев осуществляется посредством теплообменника, нагреваемого работающей горелкой, расположенной под змеевиком. Проточная колонка включается при открытии крана ГВС и выключается после его закрытия.
- Тип горелки — водонагреватели делятся на два класса: с открытой (атмосферные) и закрытой (турбированные) камерой сгорания. Первые работают без электричества, вторые энергозависимы. Существует еще несколько различий:
- Атмосферная горелка — классическая модель с открытой камерой сгорания. Воздух поступает на горелку посредством естественной циркуляции.
 Преимущества: полная энергонезависимость, небольшая стоимость. Минусы: огонь контактирует с воздухом в помещении, некоторые жалуются на запах газа при сжигании пропана посредством атмосферной горелки.
Преимущества: полная энергонезависимость, небольшая стоимость. Минусы: огонь контактирует с воздухом в помещении, некоторые жалуются на запах газа при сжигании пропана посредством атмосферной горелки. - Турбированная горелка — топливо сжигается в закрытой камере сгорания. Забор воздуха осуществляется принудительно, посредством вентилятора. Присутствует принудительная тяга. Продукты сгорания отводятся через коаксиальную трубу, поэтому колонки фактически монтируются без дымохода.
Колонки энергозависимы и не могут работать без электричества, что остается главным минусом внутреннего устройства. Присутствует функция модуляции пламени, работу контролирует электронный блок управления. Турбированными колонками удобно пользоваться, они экономно расходуют газ, что достаточно важно при использовании пропана.
- Атмосферная горелка — классическая модель с открытой камерой сгорания. Воздух поступает на горелку посредством естественной циркуляции.
- Тип установки — проточные водонагреватели: настенные. Корпус навешивают в подходящем месте на любую прочную поверхность из полнотелого строительного материала. Накопительные бойлеры выпускаются с возможностью напольного и настенного монтажа.

- Принцип розжига — водонагреватели делятся на автоматическое и полуавтоматическое оборудование. Колонка с автовключением срабатывает на открытие крана ГВС. Включается электронный розжиг пламени (от батареек или гидротурбины). После отключения воды горелка затухает. Полуавтоматические модели имеют фитиль, зажигаемый вручную или пьезоэлементом. Запальник постоянно горит и используется для розжига основной горелки.
После выбора по техническим и эксплуатационным характеристикам можно переходить к подбору подходящей модели водонагревателя по производителю. Ниже представлен рейтинг колонок, составленный в зависимости от отзывов потребителей.
Модели газовых проточных водонагревателей под сжиженный газ:
- BOSCH WR 10-2P — отличается компактными размерами и безупречным качеством сборки. Присутствует функция модуляции пламени с поддержанием постоянной температуры воды на выходе, независимо от давления в трубопроводе. Используется атмосферная горелка. Максимальный расход топлива не более 1,5 кг/час.

- Neva 4510 — автоматическая колонка с электронным розжигом и возможностью работы на природном и сжиженном газе. Пропускная способность 8 л/мин., что достаточно для одновременного обеспечения потребностей ГВС для одной точки водоразбора. Модель популярна благодаря хорошему качеству сборки и бюджетной стоимости.
- Ariston NEXT EVO SFT 11 NG EXP — бездымоходная турбированная колонка. Присутствуют встроенные функции: интеллектуальной самодиагностики, защиты от замерзания, учета расходуемой воды (при наполнении ванны подается звуковой сигнал). Подключение к бытовой электросети 220В. Производительность 11л/мин.
- Baxi SIG-2 14i — производительный проточный водонагреватель для одновременного пользования сразу двумя точками водоразбора. Внутренние функции: электрический автоматический розжиг, система ионизации пламени. Расход газа при максимальной нагрузке 2,14 кг/час. Пропускная способность 12,6 л/мин.
- SUPERLUX DGI 10L — атмосферная колонка с автоматическим розжигом и возможностью работы на сжиженном и природном газе.
 Присутствуют минимальные функции: механический блок управления, опция переключения режимов «зима-лето».
Присутствуют минимальные функции: механический блок управления, опция переключения режимов «зима-лето». - Rinnai RW-24BF — экономичная турбированная колонка с регулируемым вентилятором, для обеспечения полного сжигания газа. Автоматически поддерживается температура нагрева воды от 37-70°С. Пропускная способность 15л/мин.
Модели накопительных водонагревателей под пропан:
- Ariston SGA 200 — бойлер с емкостью на 200 л. Сжигание газа осуществляется при помощи естественной тяги. Нагрев первой порции воды до 45° происходит за 73 мин, после чего температура поддерживается в автоматическом режиме. В наличии отводы для подключения системы рециркуляции.
- Bradford White M-I-504S6FBN — накопительная емкость на189 л. Мощность 14,7 кВт. Бак имеет стеклокерамическое защитное покрытие, установлена система, предотвращающая образование накипи. Для напольной установки.
- Ariston SGA 120 — бойлер для настенного монтажа. Объем накопительной емкости 115 л. Есть защита от накипи, многоуровневая система безопасности.

Проточные газовые водонагреватели с возможностью работы от сжиженного газа выпускаются зарубежными и отечественными компаниями. Накопительные бойлеры изготавливаются исключительно за рубежом.
Какого объема выбрать газовый баллон
Если исходить исключительно из текущих расходов пропана, то будет достаточно установить один 50 л баллон. Даже при неэкономном потреблении сжиженного газа, топлива должно хватить на 10-15 дней. И это, при условии большой семьи из 4-5 человек. В техническом паспорте водонагревателей указано, что газового баллона на 50 л хватает на 10-12 часов беспрерывной работы.
Специалисты рекомендуют подключать колонку на пропане через рампу. Так, можно снизить нагрузку при работе газовой колонки от одного на несколько газовых баллонов, равномерно распределив потребление топлива и предотвратив промерзание стенок и редуктора. Подключение через рампу позволяет установить несколько емкостей меньшего объема по 25/40 л. Либо как вариант использовать 50 л баллоны, подсоединенные в связке друг с другом.
{banner_downtext}
Вес и внутренний объём газовых баллонов | ||||
Объём (л) | 5 | 12 | 27 | 50 |
Масса пустого баллона (кг) | 4 | 5,5 | 14,5 | 22,0 |
Масса баллона с пропаном (кг) | 6 | 11 | 25,9 | 43,2 |
Масса газа (кг) | 2 | 5,5 | 11,4 | 21,2 |
Высота баллона (мм) | 290 | 500 | 600 | 930 |
Диаметр баллона (мм) | 200 | 230 | 299 | 299 |
Объём газа в баллоне в зависимости от ёмкости | ||||
Ёмкость баллона (л) | 5 | 12 | 27 | 50 |
Вместимость газа (м³) | 0,95 | 2,59 | 5,38 | 10,01 |
Объём жидкого пропана (л) | 4,3 | 10,2 | 22,9 | 42,5 |
youtube.com/embed/sKpDPvpu6IE?feature=oembed» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Как подключить колонку к газовому баллону
При монтаже учитывают особенности хранения и сжигания пропана. Колонка будет работать от баллонного газа только при понижении давления на подаче до 0,2-0,3 мБар, замене форсунок. Важно предотвратить промерзание баллонов. Для обеспечения описанных условий подключение газовой колонки на сжиженном газе осуществляется в согласии со следующей схемой:
- баллоны подключаются через рампу, по несколько от 2-4 шт.;
- для нормализации давления устанавливается регулируемый редуктор.
Если подключить газовый баллон к газовому проточному или накопительному водонагревателю, по описанной выше схеме, заменить жиклеры на фитиле и форсунки на основной горелке, отрегулировать подачу топлива и воды, можно добиться стабильной работы колонки после переоборудования на пропан.
расход, проточная колонка для дачи без дымохода
Каждый, кто столкнулся с перебоями или отсутствием горячего водоснабжения, задумывается о приобретении нагревателя. Оптимальным выбором для многих наших соотечественников является проточный нагревательный прибор, который работает на газе. Хотя в большинстве случаев такие устройства используют для своей работы природный газ, существуют модели, способные функционировать на сжиженном газе.
Принцип работы
Нагрев воды в колонке, работающей на сжиженном газе, производится во время ее протекания по теплообменнику, на который воздействует тепло от горелки. Пока вода течет внутри аппарата, ее температура повышается, в результате чего из крана поступает горячая вода практически сразу после включения колонки.
Расход
На затраты газа во время работы колонки влияют многие характеристики аппарата, и в первую очередь, это мощность устройства. В среднем, если оборудование расходует около 2,3 м³ природного газа в час, то траты сжиженного газа будут составлять лишь 0,8 м³ за час.
Может ли использоваться без дымохода?
В нынешнее время покупателям доступны модели колонок, не требующие наличия вертикального дымохода. Их называют турбированными и основным отличием таких колонок является принудительная вентиляция через коаксиальную трубу, которую можно через стену вывести на улицу. Через эту трубу одновременно удаляются продукты сгорания из колонки и подкачивается воздух с улицы.
С закрытой камерой сгорания
У большинства водонагревателей, использующих в своей работе газ, камера сгорания открытая, но продаются также модели и с камерой закрытого типа. В такую колонку воздух попадает с улицы, а не из помещения, в котором установлен аппарат. В результате кислород в помещении не выжигается.
В такую колонку воздух попадает с улицы, а не из помещения, в котором установлен аппарат. В результате кислород в помещении не выжигается.
Подходит ли для дачи?
Колонка, которая в качестве источника энергии использует сжиженный газ, считается хорошим выбором для дачных условий. В отличие от природного газа и электричества, доступ к сжиженному газу на даче есть всегда, а потребности в получении горячей воды на природе и вдали от централизованного водоснабжения стабильно высокие.
Инструкция по эксплуатации
Ни в коем случае не храните баллон со сжиженным газом ни под прямыми лучами солнца, ни рядом с любым нагревательным прибором. Это также касается и прокладывания шланга от баллона к колонке. Также запрещено нагревать газовый баллон или использовать колонку, когда баллон поврежден. Немаловажно также следить, чтобы к баллону не было доступа у детей или посторонних.
Немаловажно также следить, чтобы к баллону не было доступа у детей или посторонних.
Возможно ли переналадить колонку на другой вид и давление газа?
Многие колонки можно наладить для использования сжиженного газа, однако этим обязательно должна заниматься сервисная организация с соответствующим сертификатом. Кроме того, переналадка обязательно проводится лишь с использованием комплекта деталей от производителя колонки.
Работы по переналадке включают замену жиклеров (сопел) коллектора, чтобы в результате на аппарате были установлены сопла, диаметр отверстий которых будет подходить для нужного вида газа и его давления. На время переналадки устройство обязательно отключается, а запорный кран газопровода перекрывается. Закончив переналадку, следует оценить герметичность всех соединений. Кроме того, вид газа, дату переналадки и организацию, которая ее выполнила, указывают на аппарате и в его инструкции.
Запуск и работу водонагревателя работающего на сжиженном газе смотрите в следующем видео на примере газового котла.
Установка и монтаж
Как только колонка будет настроена на работу на сжиженном газе, вам следует уделить внимание характеристикам баллона с газом:
- На нем непременно должен присутствовать редуктор, при этом его давление стабилизации должно составлять 300 мм вод.ст..
- Минимальное значение производительности паровой фазы у баллона должно составлять 1 м³ в час.
Кроме того, следует подобрать гибкий шланг с внутренним диаметром минимум 12 мм и длиной до 2,5 м. Этот шланг должен выдерживать воздействие используемого газа с учетом заданной температуры и заданного давления. Для этого подбирается сертифицированный для работы на сжиженном газе шланг. Во время подключения его нельзя скручивать и сгибать рядом с наконечниками.
Для этого подбирается сертифицированный для работы на сжиженном газе шланг. Во время подключения его нельзя скручивать и сгибать рядом с наконечниками.
Если шланг требуется установить с изгибом, то радиус такого изгиба не должен быть меньше 90 мм по его внешней черте, а начинаться изгиб должен минимум через 50 мм от наконечника. Чтобы избежать появления изломов, пользуйтесь переходниками и угловыми соединениями, а если шланг слишком длинный, его монтаж допускает применение промежуточных опор.
Разобравшись со шлангом, перед колонкой устанавливается газовый запорный кран, к которому должен быть легкий доступ. Когда монтаж завершен, обязательно проверяются все участки соединений и весь шланг, чтобы вовремя выявить негерметичность и утечку.
Газовый проточный водонагреватель EDISSON H 20 DL (сжиженный газ) — Газовые колонки проточные
ЕСТЬ быстрая доставка, рассрочка, честная гарантия и скидки! — просто позвоните! Тел. 225-07-19. Мы Вас ждём!
225-07-19. Мы Вас ждём!
Проточные водонагреватели, работающие от сети магистрального газа – самый экономичный и доступный тип оборудования для создания системы ГВС в доме или квартире. Модели серии HEAT от торговой марки EDISSON характеризуются надежностью и практичностью в использовании, благодаря наличию многоступенчатой системы защиты. Модели выполнены в плоском настенном корпусе..
EDISSON (Эдисон) H 20 DL – газовая колонка современного образца, работающая на сжиженном баллонном газе. Модель отличается надежностью и практичностью, в арсенале функций предусмотрен режим Зима-Лето. Датчик протока воды отключает подачу газа при недостаточном давлении. Розжиг горелки – электронный.
Особенности и преимущества:
- Лужёный теплообменник весом 1,9 кг
- Регулировка протока воды/подачи газа
- Электронный розжиг горелки
- Многоступенчатая система защиты
- Переключатель режимов «зима/лето
- Узкий корпус
- Надежный водогазовый узел
Честная гарантия — всё под замену. Уверены в качестве своего товара. Сломается — поменяем!
Уверены в качестве своего товара. Сломается — поменяем!
Технические характеристики
| Тип монтажа | вертикальный |
| Мощность, кВт | 20 |
| Производительность, л/мин (∆t=25℃) | 10 |
| Размеры (ШxГxВ), мм |
34x14x59
|
| Вес прибора, кг | 8 |
Строителям, работникам снабжения, дизайнерам предоставляются особые условия покупки. Уточняйте, звоните.
На сайте представлена РРЦ (цена от Производителя), мы не можем указать её ниже, зато можем сделать Вам скидки, например, на установку — Звоните! По цене и доставке договоримся
.
Комплекты для колонок BOSCH
Показать:
15255075100
Сортировка:
По умолчаниюНазвание (А — Я)Название (Я — А)Цена (низкая > высокая)Цена (высокая > низкая)Рейтинг (начиная с высокого)Рейтинг (начиная с низкого)Модель (А- Я)Модель (Я — А)
Комплект инжекторов (форсунок) с горелкой в сборе предназначен для перевода газовых колонок BOSCH W 10 KB, на сжиженный баллонный газ (пропан-бутан)
. .
.
7250.00 р.
Комплект инжекторов (форсунок) с горелкой в сборе предназначен для перевода газовых колонок BOSCH W 10 KB, на сжиженный баллонный газ (пропан-бутан)
..
7250.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR10-2P, на сжиженный баллонный газ (пропан-бутан)
..
2920.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR10-2P, на сжиженный баллонный газ (пропан-бутан)
. .
.
2920.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 GWH 13-2 CO B/H, на сжиженный баллонный газ (пропан-бутан)..
2490.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR13-2P, на сжиженный баллонный газ (пропан-бутан)
..
3970.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR13-2P, на сжиженный баллонный газ (пропан-бутан)
. .
.
2630.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR15-2P, на сжиженный баллонный газ (пропан-бутан)
..
4070.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 WR15-2P, на сжиженный баллонный газ (пропан-бутан)
..
4070.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 GWH 10-2 CO B/H, на сжиженный баллонный газ (пропан-бутан). .
.
3830.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH 23—>31 GWH 15-2 CO B/H, на сжиженный баллонный газ (пропан-бутан)..
4270.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH WT 13 AM1E, на сжиженный баллонный газ (пропан-бутан)..
2430.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH WTD 12 AME, на сжиженный баллонный газ (пропан-бутан)
. .
.
6220.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH WTD 15 AME, на сжиженный баллонный газ (пропан-бутан)
..
6920.00 р.
Комплект инжекторов (форсунок) предназначен для перевода газовых колонок BOSCH WTD 18 AME, на сжиженный баллонный газ (пропан-бутан)
..
8540.00 р.
Перевод котла на сжиженный газ — Ремонт газовых колонок в СПБ
Вы построили дом, но в вашем районе не предусмотрено магистральное газоснабжение? Газовщики обещали, что к Вашему участку подведут газ до зимы, но так этого и не сделали?Что делать? Мы предлагаем перевод котла на сжиженный газ как лучшую альтернативу
Нередко случается так, что, вышеописанные ситуации осложняются тем что Вы уже смонтировали систему отопления, работающую на магистральном газе, сделали отделку помещений, подключили систему водоснабжения и уже планировали вселяться в свой новый дом, но газа нет, а холода уже вот-вот наступят.
Что же делать в данной ситуации?
Мы рекомендуем использовать природный газ как временный или постоянный энергоноситель.
В случае если газ в скором времени должны подключить можно использовать газовые баллоны. При этом их не обязательно покупать. На сегодняшний день существует множество компаний, сдающих оборудование в аренду, оказывая сопутствующие услуги по замене пустых баллонов на заправленные. Выглядит такое решение следующим образом:
Когда подключат магистральный газ, Вам останется сдать газобаллонное оборудование, не переживая о том, что же теперь с ним делать, как это было бы в случае его покупки.
Если магистрального газа не предвидится, оптимальным вариантом будет установка газгольдера.
Множество газовых котлов могут работать как на сжиженном, так и на магистральном газе. Именно такие котлы стоит в первую очередь рассматривать в случае если газ в скором времени будет, но когда, точно не известно.
Для того чтобы котел мог работать на сжиженном газе, необходимо произвести работы по переводу котла с одного типа топлива на другой, его настройке и вводу в эксплуатацию.
Перевод котла на сжиженный газ
Процесс перевода котла отопления с одного типа топлива на другой начинается с замены форсунок. Как правило, изначально, в котлы устанавливаются форсунки для работы их на магистральном газе.
Помните, комплект форсунок для перевода на сжиженный газ является дополнительным оборудованием и приобретается отдельно!
Операцию по переводу котла на другой тип топлива лучше всего доверить специалистам, имеющим опыт в монтаже котельного оборудования. Ошибки при монтаже, влекут за собой некорректную работу оборудования, которая в свою очередь может повлечь за собой выход его из строя.
После того, как вы приобрели комплект перевода котла на сжиженный газ, необходимо осуществить его монтаж. Для этого нужно демонтировать установленные в котел форсунки для магистрального газа и на их место установить компоненты, входящие в комплект перевода на сжиженный газ.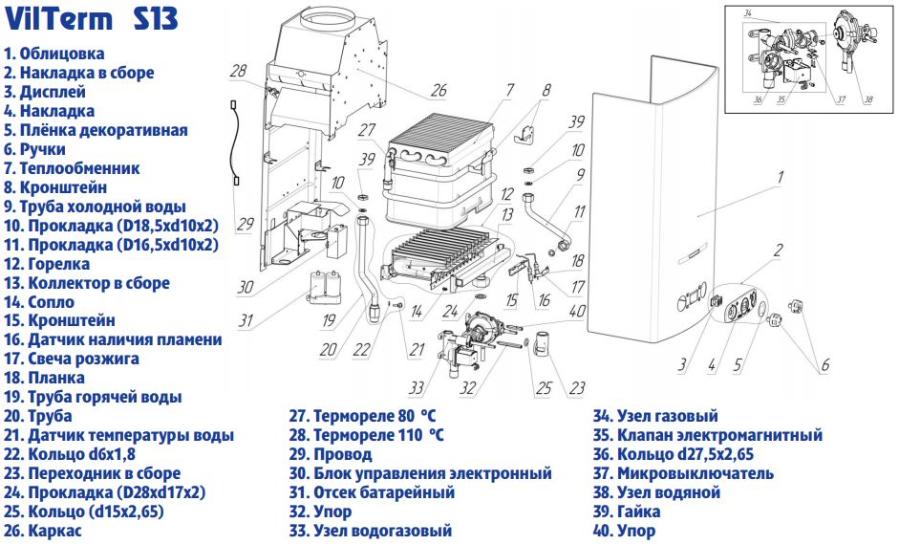
Следующим шагом производится настройка подачи газовоздушной смеси в котел, после чего осуществляется настройка автоматики и других рабочих параметров котельного оборудования.
Все вышеописанные операции являются обязательными и нужны для того чтобы котел работал в оптимальном режиме.
Неправильно настроенный котел не выдает максимального КПД и может расходовать на порядок больше топлива!
Стоимость работ по переводу котла на сжиженный газ
Для настройки котла наши специалисты используют специализированный инструмент, рекомендованный ведущими производителями котельного оборудования.
| № | Наименование услуги | ед. | Цена |
|---|---|---|---|
| 1 | Перевод на сжиженный газ котла мощностью до 30кВт | шт. | 5 000 |
| 2 | Перевод на сжиженный газ котла мощностью до 60кВт | шт. | 6 500 |
| 3 | Перевод на сжиженный газ котла мощностью свыше 60кВт | шт. | индивидуально |
Полный прайс лист с ценами на перевод
Если вам нужна консультация по подбору необходимого котельного оборудования или вы хотите перевести котел на сжиженный газ, но не знайте с чего начать, Вы всегда можете обратиться к нашим техническим специалистам за квалифицированной помощью!
15 лучших газовых колонок — Рейтинг 2021 года (Топ 15)
Если так случилось, что в вашем доме нет горячего водоснабжения, но есть газ, значит, вам нужна газовая колонка для нагрева воды. Специалисты «Эксперта цен» проанализировали модели газовых колонок, которыми больше всего интересовались покупатели в конце 2020 — начале 2021 года, и выбрали 15 самых лучших. Сейчас вы узнаете о них. Но сначала выберем фирму-производителя.
Газовая колонка какой фирмы лучше?
Лидирующие позиции по популярности, надёжности и качеству сборки на сегодняшний день занимают газовые водонагреватели чешского производителя Mora Top. Его продукция никогда не залёживается в магазинах долго, а потому иногда надо просто успеть сделать заказ. Среди иностранных производителей газовых колонок не отстают всегда востребованные бренды Bosch и Ariston. Продукцию с неплохим соотношением цены и качества предлагают на российском рынке Zanussi и Hyundai. Лучшие отечественные производители традиционно представлены газовыми колонками марок Нева и Ладогаз.
Его продукция никогда не залёживается в магазинах долго, а потому иногда надо просто успеть сделать заказ. Среди иностранных производителей газовых колонок не отстают всегда востребованные бренды Bosch и Ariston. Продукцию с неплохим соотношением цены и качества предлагают на российском рынке Zanussi и Hyundai. Лучшие отечественные производители традиционно представлены газовыми колонками марок Нева и Ладогаз.
Полезные советы для обеспечения долгой и надёжной работы газовых колонок
- Установка и подключение должны осуществляться квалифицированными специалистами. Часто от того, как настроена газовая колонка, зависит качество её работы.
- Необходимо регулярно производить очищение запальника и теплообменника от продуктов горения (странно обвинять в засорах колонку). Это заметно продлит «срок жизни» прибора.
- В старых домах со слишком заниженным давлением воды в системе лучше устанавливать специальные насосы. При стабильном давлении воды автоматический запуск происходит без проблем, а температура нагрева будет поддерживаться более корректно.

- Необходимо соблюдать важные рекомендации от производителя, указанные в инструкции пользователя.
Правильно выбирайте модель колонки в зависимости от требуемого или желаемого количества горячей воды. В принципе, конструктивно современные газовые проточные водонагреватели лишь условно можно поделить на версии для одной, двух или больше точек водоразбора. Дело скорее в заявленной максимальной производительности. Простое правило: меньше 12-13 л/мин – один кран или поочерёдное использование, больше – хватит на два или на несколько.
Рейтинг лучших газовых колонок
И напоследок… Какую газовую колонку лучше купить?
Все газовые водонагреватели из нашего рейтинга достаточно надежны, безопасны, находятся примерно в одной ценовой категории. Можно смело утверждать, что все они хорошо работают при правильной установке и эксплуатации. Многие проблемы, на которые жалуются владельцы колонок, решаются простой заменой батареек и чисткой дымохода. Важно — если в вашем регионе вода жесткая, то лучше поставить фильтр. Иначе образуется накипь, которая забивает теплообменник, и газовая колонка гораздо быстрее ломается. Если нет фильтра, учитывайте, что накипь образуется при высокой температуре (от 40 градусов) — не перегревайте прибор.
Важно — если в вашем регионе вода жесткая, то лучше поставить фильтр. Иначе образуется накипь, которая забивает теплообменник, и газовая колонка гораздо быстрее ломается. Если нет фильтра, учитывайте, что накипь образуется при высокой температуре (от 40 градусов) — не перегревайте прибор.
Проявляются недостатки газовых колонок часто из-за того, что пользователи не соблюдают требования инструкции (или вообще ее не читают). Очень рекомендуем следовать правилам! Еще помните, что газовый водонагреватель нужно настраивать (заводские настройки предназначены для тестового запуска, не для всех условий подходят), и делать это должны специалисты.
Наконец, актуальное для тех, кто не знает, напутствие на случай поломки газовой колонки до истечения срока гарантии: коли уполномоченные производителем сервисные службы по каким-то причинам отказываются решать проблему, сильно затягивают ремонт, ссылаясь на отсутствие запчастей, либо авторизированные СЦ попросту отсутствуют в населённом пункте, где приобретался водонагреватель, потребитель вправе потребовать «сатисфакции» непосредственно у магазина. В отсутствие нормального сервиса любой недостаток товара, если дефект окажется гарантийным, автоматически становится «существенным». И можно потребовать обмен или возврат денег (в том числе возмещения затрат на монтаж/демонтаж).
В отсутствие нормального сервиса любой недостаток товара, если дефект окажется гарантийным, автоматически становится «существенным». И можно потребовать обмен или возврат денег (в том числе возмещения затрат на монтаж/демонтаж).
Удачной покупки!
Биоконверсия природного газа в жидкое топливо: возможности и проблемы
Реферат
Природный газ представляет собой смесь низкомолекулярных углеводородных газов, которые могут быть получены из ископаемых или антропогенных ресурсов. Хотя природный газ используется в качестве транспортного топлива, ограничения в хранении, относительно низкое энергосодержание (МДж / л) и доставка имеют ограниченное широкое распространение. Было исследовано расширенное использование природного газа для производства биотоплива микроорганизмами.В последние годы аэробная биоконверсия природного газа (или, в первую очередь, метана, содержащегося в природном газе) в жидкое топливо (Bio-GTL) с помощью биокатализаторов (метанотрофов) привлекает все большее внимание как многообещающая альтернатива для производства биотоплива без дополнительных затрат. Метанотрофные бактерии способны превращать метан в липиды микробов, которые, в свою очередь, могут быть преобразованы в возобновляемое дизельное топливо с помощью процесса гидроочистки. В этой статье обобщены биоразнообразие, каталитические свойства, ключевые ферменты и пути распространения этих микробов.Технологии биопроцессов обсуждаются на основе существующей литературы, включая условия культивирования, режимы ферментации, конструкцию биореактора, а также экстракцию и обновление липидов. В этом обзоре также описывается потенциал Bio-GTL с использованием метана в качестве альтернативного источника углерода, а также основные проблемы и будущие потребности в исследованиях накопления микробных липидов, полученных из метана, ключевого показателя эффективности и технико-экономического анализа. Анализ затрат на сырье показывает, что дизельное топливо, полученное из метана, потенциально может быть конкурентоспособным с дизельным топливом, полученным из нефти.
Метанотрофные бактерии способны превращать метан в липиды микробов, которые, в свою очередь, могут быть преобразованы в возобновляемое дизельное топливо с помощью процесса гидроочистки. В этой статье обобщены биоразнообразие, каталитические свойства, ключевые ферменты и пути распространения этих микробов.Технологии биопроцессов обсуждаются на основе существующей литературы, включая условия культивирования, режимы ферментации, конструкцию биореактора, а также экстракцию и обновление липидов. В этом обзоре также описывается потенциал Bio-GTL с использованием метана в качестве альтернативного источника углерода, а также основные проблемы и будущие потребности в исследованиях накопления микробных липидов, полученных из метана, ключевого показателя эффективности и технико-экономического анализа. Анализ затрат на сырье показывает, что дизельное топливо, полученное из метана, потенциально может быть конкурентоспособным с дизельным топливом, полученным из нефти.
Ключевые слова
Биоконверсия природного газа в жидкое топливо (Bio-GTL)
Парниковый газ
Возобновляемое дизельное топливо
Метанотрофные бактерии
Микробные липиды
Оптимизация биопроцессов
Экстракция липидов
экономический анализ
Рекомендуемые статьиЦитирующие статьи (0)
Copyright © 2014 Авторы. Опубликовано Elsevier Inc.
Опубликовано Elsevier Inc.
Рекомендуемые статьи
Цитирующие статьи
Инженеры разработали метод преобразования природного газа в твердое вещество
Инженеры Национального университета Сингапура разработали новый метод преобразования природного газа в твердую форму, который позволяет его хранить и транспортировать более легко и безопасно.Преобразование материала из газа в твердое вещество требует всего 15 минут и использует малотоксичную смесь. Новый метод конверсии имеет большое значение, потому что, хотя многие страны по всему миру стремятся отказаться от ископаемого топлива, природный газ по-прежнему широко используется в большинстве стран мира.
Природный газ часто превращается в жидкость, чтобы с ним было легче работать, но процесс преобразования требует чрезвычайно низких температур, составляющих около -260 градусов по Фаренгейту. Новый метод превращает газ в твердое тело, и исследователи отмечают, что природа уже преобразует газ в твердое тело при определенных условиях. Молекулы природного газа могут попасть в «клетки» молекул воды, образуя газовые гидраты или горючий лед.
Молекулы природного газа могут попасть в «клетки» молекул воды, образуя газовые гидраты или горючий лед.
Однако этот процесс может происходить в природе за миллионы лет. Исследователи ускорили процесс, заявив о самом быстром времени конверсии за всю историю. Ключ к прорыву — это аминокислота под названием L-триптофан, которая ускоряет скорость реакции и быстрее улавливает больше газа в твердые гидраты. Весь процесс занимает 15 минут, что более чем в два раза быстрее, чем по текущему стандарту.
Полученное твердое вещество удобнее и безопаснее хранить и транспортировать. Как кусок льда, газ сокращается в объеме в 90 раз, он невзрывоопасен и достаточно стабилен, чтобы его можно было хранить в обычной морозильной камере при температуре 23 градуса по Фаренгейту. Этот метод также требует менее токсичных добавок, чем обычно.
Процесс был протестирован только в лаборатории, но команда намеревается провести экспериментальный эксперимент по переработке около 220 фунтов газа в день. В конце концов, команда надеется расширить процесс до промышленного использования.
В конце концов, команда надеется расширить процесс до промышленного использования.
Единицы газа
Газовые установки
Вопреки распространенному мнению, газ обычно продается не за единицу объема, а за единицу энергии, которая может быть произведена путем сжигания газа. Конечные потребители газа заинтересованы в тепловой энергии, выделяемой при сжигании газа. Поскольку тепловая энергия газа связана с относительной долей «более легкого» метана по сравнению с «более тяжелым» этаном, пропаном, бутаном, пентаном и другими компонентами, тепловая энергия не является постоянной величиной для различных источников газа.
Тепловая энергия конкретного газового потока измеряется в единицах теплотворной способности, которая определяется количеством единиц тепла, выделяемых при сгорании единицы объема газа. Типичными единицами теплотворной способности являются британские тепловые единицы (британские тепловые единицы), джоули (Дж) и килокалории (ккал).
Большинство промышленных и бытовых потребителей получают газ через трубопровод и газовый счетчик, который измеряет объем поставленного газа. Это измерение объема впоследствии преобразуется с использованием средней теплотворной способности на коэффициент объема в количество единиц энергии, потребленных конечным пользователем, и умножается на цену за единицу энергии для определения суммы, выставленной в счет.
Это измерение объема впоследствии преобразуется с использованием средней теплотворной способности на коэффициент объема в количество единиц энергии, потребленных конечным пользователем, и умножается на цену за единицу энергии для определения суммы, выставленной в счет.
Во всем мире стоимость газа для потребителя обычно указывается в долларах за британскую тепловую единицу. Британская тепловая единица — это энергия, необходимая для повышения температуры 1 фунта воды на 1 ° F. Для более крупных промышленных потребителей чаще используются сокращения MBtu (тысяча или 10 3 Btu) или MMBtu (миллион или 10 6 Btu). В Соединенном Королевстве за газ взимается плата с бытовых потребителей по цене за термостат, что эквивалентно 100 000 британских тепловых единиц.
Объемы газа обычно измеряются в кубических футах ( 3 футов) или кубических метрах ( 3 м).Запасы газа выражаются в миллиардах кубических футов (bcf) (10 9 ) или триллионах кубических футов (tcf) (10 12 ), или, в случае стран, использующих метрическую систему, в миллиардах кубических метров (bcm) . Объем произведенного или потребленного газа часто выражается в миллионах кубических футов (MMcf), (10 6 ) и Mcf (тысячах кубических футов). Объем газа также может быть выражен в миллионах кубических футов в день (MMcfd), иногда записывается как MMscfd для обозначения стандартных условий, и его метрический аналог, миллиард кубических метров в день (Bcmd).(M обычно используется для обозначения 1000, что основано на римской системе счисления. Таким образом, MM обозначает 1000 x 1000 или 1 миллион (10 6 ). В метрической системе k также обозначает 1000. В энергетической отрасли используется и M, и k. Некоторые компании используют строчную букву m для обозначения 1000; таким образом, mmcfd будет равно MMcfd.
Объем произведенного или потребленного газа часто выражается в миллионах кубических футов (MMcf), (10 6 ) и Mcf (тысячах кубических футов). Объем газа также может быть выражен в миллионах кубических футов в день (MMcfd), иногда записывается как MMscfd для обозначения стандартных условий, и его метрический аналог, миллиард кубических метров в день (Bcmd).(M обычно используется для обозначения 1000, что основано на римской системе счисления. Таким образом, MM обозначает 1000 x 1000 или 1 миллион (10 6 ). В метрической системе k также обозначает 1000. В энергетической отрасли используется и M, и k. Некоторые компании используют строчную букву m для обозначения 1000; таким образом, mmcfd будет равно MMcfd.
Как указывалось ранее, преобразование объема в энергию требует знания средней теплотворной способности конкретного газа. Природный газ из разных месторождений, а иногда и из разных пластов одного и того же месторождения, может иметь разные пропорции углеводородных компонентов и, следовательно, различную теплотворную способность. Обычно используется коэффициент 1000 БТЕ / фут 3 .
Обычно используется коэффициент 1000 БТЕ / фут 3 .
Сырая нефть имеет теплотворную способность от 5,4 млн БТЕ до 5,8 млн БТЕ на баррель (баррель) нефти, в зависимости от состава нефти. Часто необходимо и полезно преобразовать объем газа в баррели нефтяного эквивалента в энергетическом эквиваленте, используя единицы барреля нефтяного эквивалента (бнэ). Обычно это делается, когда и нефть, и газ находятся и добываются в одном пласте, что упрощает оценку общих запасов или объемов добычи.
Онлайн-конвертер единиц газа
Инструменты для переоборудования
Единицы измерения природного газа могут сбивать с толку.Чтобы упростить конвертацию, Natgas.info создал приложение для систем iPhone / iPad и Android, а также приведенный ниже онлайн-конвертер единиц газа.
Чтобы использовать онлайн-конвертер на этом сайте, см. Ниже (если конвертер единиц не отображается ниже, значит, проблема с Adobe Flash, щелкните Конвертер единиц газа в левом столбце страницы). Для использования сначала выберите соответствующее энергосодержание на кубический фут газа и на баррель нефти.Если вы не знаете точные коэффициенты, которые следует использовать, коэффициенты 1 миллион британских тепловых единиц = 1000 кубических футов и 1 баррель нефтяного эквивалента = 5800 кубических футов являются обычным приближением.
Для использования сначала выберите соответствующее энергосодержание на кубический фут газа и на баррель нефти.Если вы не знаете точные коэффициенты, которые следует использовать, коэффициенты 1 миллион британских тепловых единиц = 1000 кубических футов и 1 баррель нефтяного эквивалента = 5800 кубических футов являются обычным приближением.
Затем выберите единицы измерения: объемы (кубические футы, метры и т. Д.), Нормы (кубические футы в день) или конечные продукты (объемы жидкостей GTL или СПГ или ватты электроэнергии). Первый калькулятор предназначен для объемов, а второй калькулятор может использоваться для ставок и конечных продуктов.
Наконец, выберите входные единицы («Входные единицы»), введите входное значение, а затем выберите желаемую выходную единицу («Выходные единицы»).Нажмите «Рассчитать», чтобы произвести преобразование.
Наслаждайтесь!
Переработка сырой нефти — процесс переработки
Как сырая нефть перерабатывается в нефтепродукты
Нефтеперерабатывающие заводы превращают сырую нефть в нефтепродукты для использования в качестве топлива для транспорта, отопления, мощения дорог и производства электроэнергии, а также в качестве сырья для производства химикатов.
Разделение
Современная сепарация включает пропускание сырой нефти через горячие печи.Образующиеся жидкости и пары отводятся в дистилляционные установки. Все нефтеперерабатывающие заводы имеют установки атмосферной дистилляции, в то время как более сложные нефтеперерабатывающие заводы могут иметь установки вакуумной дистилляции.
Внутри дистилляционных установок жидкости и пары разделяются на нефтяные компоненты, называемые фракциями в соответствии с их точками кипения. Тяжелые фракции находятся внизу, а легкие — вверху.
Самые легкие фракции, в том числе бензин и сжиженные нефтеперерабатывающие газы, испаряются и поднимаются на верхнюю часть дистилляционной колонны, где снова конденсируются в жидкости.
Жидкости средней массы, включая керосин и дистилляты, остаются в середине дистилляционной колонны.
Более тяжелые жидкости, называемые газойлем, отделяются внизу в дистилляционной колонне, в то время как самые тяжелые фракции с самыми высокими температурами кипения оседают на дне колонны.
Преобразование
После перегонки тяжелые фракции перегонки с более низкой стоимостью могут быть переработаны в более легкие и более ценные продукты, такие как бензин.Здесь фракции из установок перегонки преобразуются в потоки (промежуточные компоненты), которые в конечном итоге становятся готовыми продуктами.
Наиболее широко используемый метод конверсии называется крекингом , потому что он использует тепло, давление, катализаторы и иногда водород для расщепления тяжелых углеводородных молекул на более легкие. Установка крекинга состоит из одного или нескольких высоких, толстостенных реакторов в форме ракеты и сети печей, теплообменников и других сосудов.Комплексные нефтеперерабатывающие заводы могут иметь один или несколько типов крекинг-установок, включая установки каталитического крекинга с псевдоожиженным слоем и установки гидрокрекинга / гидрокрекинга.
Крекинг — не единственная форма переработки сырой нефти. Другие процессы нефтепереработки перестраивают молекулы для увеличения стоимости, а не для расщепления молекул.
Ректификационная установка каталитического крекинга
Источник: Chevron (защищено авторским правом)
Рабочие нефтепереработки над нефтеперерабатывающим заводом
Источник: Chevron (защищено авторским правом)
При алкилировании, например, компоненты бензина получают путем объединения некоторых газообразных побочных продуктов крекинга.Процесс, который, по сути, является обратным растрескиванием, происходит в серии больших горизонтальных сосудов и высоких тощих башен.
При риформинге используется тепло, умеренное давление и катализаторы для превращения нафты, легкой, относительно невысокой фракции, в высокооктановые компоненты бензина.
Лечение
Последние штрихи выполняются во время окончательной обработки. Чтобы произвести бензин, специалисты нефтеперерабатывающего завода тщательно комбинируют различные потоки от технологических установок.Уровень октана, номинальное давление паров и другие особые факторы определяют смесь бензина.
Хранилище
Как поступающая сырая нефть, так и исходящие конечные продукты временно хранятся в больших резервуарах на резервуарном парке рядом с нефтеперерабатывающим заводом. Трубопроводы, поезда и грузовики доставляют готовую продукцию из резервуаров для хранения в другие места по всей стране.
Последнее обновление: 23 сентября 2020 г.
Universal Industrial Gases, Inc…. Конверсия единиц аргона (газ, жидкость)
Universal Industrial Gases, Inc. … Конверсия единиц аргона (газ, жидкость)
Данные преобразования единиц для аргона
| Вес | Газ | Жидкость | ||||
| фунтов стерлингов (фунты) | килограммы (кг) | кубических футов (scf) | м3 (Нм 3 ) | галлонов (галлон) | литров (л) | |
| 1 фунт | 1. 0 0 | 0,4536 | 9,671 | 0,2543 | 0,08600 | 0,3255 |
| 1 килограмм | 2.205 | 1.0 | 21,32 | 0,5605 | 0,18957 | 0.7176 |
| 1 ст.ф. | 0,1034 | 0,04690 | 1. 0 0 | 0,02628 | 0,008893 | 0,03366 |
| 1 Нм 3 газ | 3,933 | 1,7840 | 38.04 | 1.0 | 0,3382 | 1,2802 |
| 1 галлон жидкости | 11,630 | 5,276 | 112,5 | 2,957 | 1. 0 0 | 3,785 |
| 1 литр жидкости | 3.072 | 1,3936 | 29,71 | 0,7812 | 0,2642 | 1.0 |
| 1 короткая тонна | 2000 | 907,2 | 19342 | 508,6 | 172 | 651.0 |
| Scf (стандартный кубический фут) измеренный газ при 1 атмосфере и 70F.  Нм 3 (нормальный кубический метр) газ измеряется при 1 атмосфере и 0C. Жидкость измерена при 1 атмосфере и температуре кипения. |
Universal Industrial Gases, Inc.
Универсал Криогаз, ООО
3001 Emrick Blvd, Suite 320
Bethlehem, Pennsylvania 18020, USA
Телефон (610) 559-7967 Факс (610) 515-0945
Все содержащиеся здесь материалы Copyright 2003
/ 2017 UIG.
Ваш браузер не поддерживает скрипт
Первое трехмерное моделирование гидродинамики пузырьковой колонны открывает путь для коммерческого преобразования газа в жидкость в шламовом реакторе
Fluent Inc. Марк С. Бон, вице-президент по разработке, Rentech Inc., Денвер
Содержание
Оптимизация суспензионного реактора
Компьютерное моделирование динамики пузырькового столба
Корреляция с экспериментальными данными
Разработав трехмерное моделирование гидродинамики в реакторе с пузырьковой колонной, инженеры Rentech Inc. (Денвер) сделали важный шаг на пути к разработке эффективного суспензионного реактора для крупномасштабной конверсии синтез-газа в жидкие углеводороды. Моделирование позволяет нам определить содержание газа, ключевую переменную, влияющую на скорость реакции превращения газа в жидкость (GTL), с использованием химии Фишера-Тропша (FT).
(Денвер) сделали важный шаг на пути к разработке эффективного суспензионного реактора для крупномасштабной конверсии синтез-газа в жидкие углеводороды. Моделирование позволяет нам определить содержание газа, ключевую переменную, влияющую на скорость реакции превращения газа в жидкость (GTL), с использованием химии Фишера-Тропша (FT).
Эта информация важна, потому что существует потенциал для широкого применения FT для переработки остатков нефтепереработки, что является постоянно растущей проблемой во всем мире.Шламовый реактор предлагает один из таких методов, но он требует детального знания гидродинамики реакторов промышленного размера. Подтвержденное трехмерное вычислительное моделирование гидродинамики позволяет нам моделировать промышленный реактор.
Rentech Inc. — это 18-летняя корпорация, которая владеет, лицензирует и продает запатентованный процесс, который превращает синтез-газ, смесь водорода и окиси углерода, полученную из любого углеродсодержащего материала, в ценные жидкие углеводороды, включая дизельное топливо, нафту , и воски. В процессе Rentech используется катализатор на основе железа в суспензионном реакторе, чтобы влиять на конверсию GTL. Rentech — одна из четырех компаний в мире, эксплуатирующих промышленные установки GTL.
В процессе Rentech используется катализатор на основе железа в суспензионном реакторе, чтобы влиять на конверсию GTL. Rentech — одна из четырех компаний в мире, эксплуатирующих промышленные установки GTL.
Одна из наших целей — расширить коммерческое применение технологии GTL. Экономические выгоды от этого очевидны. Например, нефтяной кокс, остаточный материал процесса нефтепереработки, содержит определенное количество металлов и серы. Высокое содержание серы и металлов в этом нефтяном коксе обычно приводит к тому, что нефтеперерабатывающий завод присваивает материалу нулевое или даже отрицательное значение.Нефтеперерабатывающий завод, производящий 1500 тонн нефтяного кокса в день, может газифицировать кокс для производства синтез-газа и технологии GTL для создания чистых, низкосернистых и низкоароматических синтетических жидкостей с низким содержанием серы и ароматических углеводородов примерно 3000 баррелей в день, включая бензин и дизельное топливо. В зависимости от цены нефтяного кокса и стоимости жидкостей для синтеза нефтеперерабатывающий завод может рассчитывать на дополнительный доход в размере 20 миллионов долларов в год, исходя из того, что стоимость нефтяного кокса составляет 5 долларов за тонну, а синтетических жидкостей — 25 долларов за баррель.
Другим важным сырьем для конверсионных заводов, использующих технологию Rentech, является природный газ из скважин, добыча которых не ведется из-за их удаленности, природный газ, непригодный для коммерческой продажи, поскольку он содержит разбавители, такие как углекислый газ или азот, нефтяные скважины, сжигающие попутный газ, и промышленный отходящий газ.Это сырье в изобилии имеется во всем мире.
Оптимизация шламового реактора (В начало)
GTL — это двухэтапный процесс, который начинается с преобразования сырья в синтез-газ. Второй этап — реакция Фишера-Тропша, процесс, изобретенный в Германии в 1923 году. Он превращает окись углерода и водород в широкий спектр углеводородов от метана до тяжелых парафинов. Реакцию Фишера-Тропша можно проводить в реакторах различного типа.В настоящее время существует большой интерес к использованию суспензионных реакторов, поскольку они относительно недороги в строительстве и эксплуатации и обладают отличным тепло- и массообменом, что способствует высокой скорости реакции.
Суспензионный реактор — это сосуд, содержащий катализатор, суспендированный в жидком углеводороде. Синтез-газ поступает в нижнюю часть емкости и пузырится вверх через реактор. Когда пузырьки контактируют с катализатором, происходит реакция Фишера-Тропша. Гидродинамика в реакторе сложна, но понимание ее важно для достижения высокой скорости реакции, необходимой для коммерческой конверсии GTL.Для достижения высокой скорости массообмена в реакторе необходимо обеспечить хорошее распределение пузырьков газа с большой площадью поверхности раздела между пузырьками и жидкой углеводородной средой.
В прошлом исследователи пытались понять гидродинамику суспензионных реакторов, проводя лабораторные эксперименты. Недостатком использования реакторов лабораторного масштаба для понимания гидродинамики является то, что результаты не обязательно точно масштабируются. Например, реакторы малого диаметра, как известно, влияют на движение пузырьков, слияние пузырьков, а также на разрыв пузырьков через эффекты стенок.
Большинство исследователей предполагают, что движение пузырьков в реакторе большего размера будет несколько другим, но они не знают, насколько это различие. Чтобы получить точную информацию о гидродинамике шламового реактора промышленного масштаба, необходимо изучить сосуд такого размера. Однако капитальные затраты на такую физическую модель непомерно высоки.
Компьютерное моделирование динамики пузырькового столба (В начало)
Программное обеспечение вычислительной гидродинамики (CFD) предлагает многообещающий вариант для исследования гидродинамики больших суспензионных реакторов, поскольку проверенная модель малого реактора легко масштабируется.До недавнего времени CFD не использовались для изучения движения пузырей. Но в августе 1999 года исследователи из Вашингтонского университета, Сент-Луис, штат Миссури, и Ливана, штат Нью-Хэмпшир, разработчик программного обеспечения CFD, представили двухмерное моделирование динамики газа и жидкости в реакторе с пузырьковой колонной на GLS ’99: 4-я Международная конференция по газожидкостным и газожидкостным твердым веществам .
Одновременно с этим мы начали разрабатывать 3D-модель CFD для моделирования динамики пузырькового столба с помощью FLUENT. В качестве первого шага мы использовали компьютерное моделирование для расчета расширения слоя и содержания газа.Задержка газа является важным фактором скорости реакции, поскольку задержка определяет площадь поверхности раздела и, следовательно, скорость реакции. Задержка газа — одна из переменных, которые необходимо максимизировать для обеспечения высоких скоростей реакции. Компьютерное моделирование задержки газа представляет собой сложную задачу, поскольку требует отслеживания кратковременного движения каждого пузырька в трех измерениях и поскольку поток обычно является турбулентным
Первым шагом в разработке компьютерного моделирования было создание 3D-модели реактора.Для этого мы использовали GAMBIT, программный препроцессор FLUENT, который создает и моделирует геометрию. Геометрию колонны создать было несложно. По сути, это был вертикальный цилиндр с входом внизу и выходом вверху. На рис. 1 показан цилиндр, смотрящий вверх по направлению к впускному отверстию.
На рис. 1 показан цилиндр, смотрящий вверх по направлению к впускному отверстию.
После того, как модель была разработана, следующим шагом было предоставление программе граничных условий для задачи. Они включали тот факт, что стороны цилиндра были стенками, что вход в нижней части был входом для скорости, а выход наверху был выходом для давления.Поскольку модель была симметричной, а граничные условия были одинаковыми для каждой стороны, мы разрезали модель вертикально, создавая плоскость симметрии в половину. Это было сделано для сокращения времени решения. Затем мы попросили GAMBIT создать сетку. Внешняя поверхность сетки также видна на рисунке 1.
Геометрия модели и сетка
После импорта сетки в FLUENT следующим шагом было предоставление дополнительной информации о проблеме. Мы выбрали модель турбулентности k-epsilon, предоставленную программным обеспечением.Нам также нужно было указать диаметр пузырьков. Основываясь на нашей экспериментальной работе, а также на данных, представленных в литературе, мы выбрали три миллиметра. Мы указали временной шаг в 1 миллисекунду для каждой итерации анализа. Наконец, мы указали свойства жидкости (воды) и газа (воздуха).
Мы указали временной шаг в 1 миллисекунду для каждой итерации анализа. Наконец, мы указали свойства жидкости (воды) и газа (воздуха).
Мы выполнили полученное моделирование на рабочей станции Dell 410 с двумя процессорами Pentium III 600 МГц под управлением Windows NT. Двойные процессоры позволяли запускать два моделирования одновременно с небольшой потерей вычислительной эффективности.
На этом этапе мы запустили моделирование переходных процессов. Программное обеспечение требовало нескольких десятков итераций для схождения на каждом временном шаге. На рисунке 2 показан снимок распределения газа и жидкости в плоскости симметрии через 5,6 секунды. Боковое искажение газовой струи легко увидеть на контурном графике, как и расположение границы раздела газ / жидкость. Векторные графики, которые не показаны, позволили нам увидеть обратное перемешивание, вызванное движением пузырька вверх по центру колонки и возвращением жидкости наружу.
Результаты, показывающие контуры объемной доли воздуха
Мы рассчитали задержку газа, построив график распределения объемной доли газа в зависимости от высоты колонки. На графике была показана точка, в которой концентрация газа быстро увеличивалась, а именно граница раздела жидкость-газ. Это тот же метод, который мы используем при экспериментальном измерении высоты границы раздела. Следующим шагом было сравнение высоты границы раздела жидкость-газ с исходной высотой границы раздела жидкость-газ.Расширение, или степень повышения границы раздела жидкость-газ, показало, сколько газа удерживалось в реакторе, из чего легко рассчитать удержание газа.
На графике была показана точка, в которой концентрация газа быстро увеличивалась, а именно граница раздела жидкость-газ. Это тот же метод, который мы используем при экспериментальном измерении высоты границы раздела. Следующим шагом было сравнение высоты границы раздела жидкость-газ с исходной высотой границы раздела жидкость-газ.Расширение, или степень повышения границы раздела жидкость-газ, показало, сколько газа удерживалось в реакторе, из чего легко рассчитать удержание газа.
Корреляция с экспериментальными данными (В начало)
Поскольку нас интересовало корреляция содержания газа со скоростью газа на входе, мы провели моделирование с несколькими скоростями на входе и определили задержку для каждой из них. Мы сравнили наши результаты компьютерного моделирования с результатами экспериментальной работы, рис. 3, и обнаружили хорошее согласие.
Сравнение модели CFD и экспериментальных данных
Эта работа является важным шагом на пути к пониманию гидродинамики шламовых реакторов большого диаметра.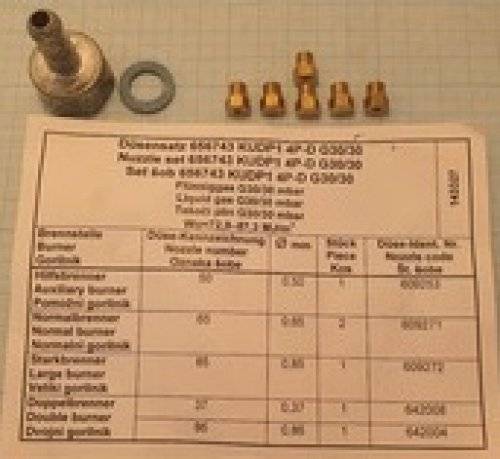 После того, как Rentech утвердит компьютерную модель, которая может моделировать все аспекты гидродинамики пузырьковой колонны, размер модели можно увеличить, чтобы ответить на аналогичные вопросы о более крупных реакторах. Когда гидродинамику этих сосудов можно будет моделировать на компьютере, можно будет использовать компьютер для оптимизации процесса, в конечном итоге достигнув скорости передачи, достаточно высокой для широкого коммерческого использования этой технологии.С потенциальной экономией в миллионы долларов на одном нефтеперерабатывающем заводе эта технология предлагает большие перспективы.
После того, как Rentech утвердит компьютерную модель, которая может моделировать все аспекты гидродинамики пузырьковой колонны, размер модели можно увеличить, чтобы ответить на аналогичные вопросы о более крупных реакторах. Когда гидродинамику этих сосудов можно будет моделировать на компьютере, можно будет использовать компьютер для оптимизации процесса, в конечном итоге достигнув скорости передачи, достаточно высокой для широкого коммерческого использования этой технологии.С потенциальной экономией в миллионы долларов на одном нефтеперерабатывающем заводе эта технология предлагает большие перспективы.
Для получения дополнительной информации: Fluent Inc., 10 Cavendish Ct., Centerra Resource Park, Ливан, NH 03766. Телефон: 603-643-2600. Факс: 603-643-3967.
Интегрированный биопроцесс для преобразования газообразных субстратов в жидкости
Значение
В поисках недорогого сырья (рентабельное производство топлива) здесь мы демонстрируем двухэтапный интегрированный биопроцесс для преобразования синтез-газа в липиды. Мы используем врожденные способности ацетогенов и исследуем концепции массопереноса газ-жидкость для создания интегрированной двухступенчатой биореакторной системы, которая может преобразовывать газы в жидкое топливо в больших масштабах. Кроме того, поскольку скорость фиксации CO 2 значительно превышает скорость образования CO 2 в двух единицах процесса, существует значительный потенциал для рециркуляции CO 2 в нашей интегрированной системе. В более широком смысле реализация этих концепций производства топлива может распространяться на ряд коммерчески важных биологических платформ, в зависимости от потенциальных источников синтез-газа или продуктов его конверсии, а именно ацетата.
Мы используем врожденные способности ацетогенов и исследуем концепции массопереноса газ-жидкость для создания интегрированной двухступенчатой биореакторной системы, которая может преобразовывать газы в жидкое топливо в больших масштабах. Кроме того, поскольку скорость фиксации CO 2 значительно превышает скорость образования CO 2 в двух единицах процесса, существует значительный потенциал для рециркуляции CO 2 в нашей интегрированной системе. В более широком смысле реализация этих концепций производства топлива может распространяться на ряд коммерчески важных биологических платформ, в зависимости от потенциальных источников синтез-газа или продуктов его конверсии, а именно ацетата.
Реферат
В поисках недорогого сырья для рентабельного производства жидкого топлива мы исследовали газообразные субстраты, которые могут быть доступны по низкой цене и в достаточно больших масштабах для промышленного производства топлива. Здесь мы представляем новую схему биоконверсии, которая эффективно преобразует синтез-газ, полученный в результате газификации угля, природного газа или биомассы, в липиды, которые можно использовать для производства биодизеля. Мы представляем интегрированный метод преобразования, состоящий из двухступенчатой системы.На первом этапе анаэробный биореактор преобразует смеси газов CO 2 и CO или H 2 в уксусную кислоту, используя анаэробный ацетоген Moorella thermoacetica . Продукт уксусной кислоты подают в качестве субстрата во второй биореактор, где он аэробно превращается в липиды с помощью модифицированных маслянистых дрожжей, Yarrowia lipolytica . Сначала мы описываем процесс, осуществляемый в каждом реакторе, а затем представляем интегрированную систему, которая производит микробное масло с использованием синтез-газа в качестве входного материала.Интегрированная лабораторная реакторная система непрерывного действия произвела 18 г / л триацилглицеридов C16-C18 непосредственно из синтез-газа с общей производительностью 0,19 г⋅л -1 ч -1 и содержанием липидов 36%. Несмотря на то, что она не оптимальна по сравнению с характеристиками отдельных компонентов реактора, представленная интегрированная система демонстрирует возможность существенной чистой фиксации диоксида углерода и преобразования газообразного сырья в липиды для производства биодизельного топлива.
Мы представляем интегрированный метод преобразования, состоящий из двухступенчатой системы.На первом этапе анаэробный биореактор преобразует смеси газов CO 2 и CO или H 2 в уксусную кислоту, используя анаэробный ацетоген Moorella thermoacetica . Продукт уксусной кислоты подают в качестве субстрата во второй биореактор, где он аэробно превращается в липиды с помощью модифицированных маслянистых дрожжей, Yarrowia lipolytica . Сначала мы описываем процесс, осуществляемый в каждом реакторе, а затем представляем интегрированную систему, которая производит микробное масло с использованием синтез-газа в качестве входного материала.Интегрированная лабораторная реакторная система непрерывного действия произвела 18 г / л триацилглицеридов C16-C18 непосредственно из синтез-газа с общей производительностью 0,19 г⋅л -1 ч -1 и содержанием липидов 36%. Несмотря на то, что она не оптимальна по сравнению с характеристиками отдельных компонентов реактора, представленная интегрированная система демонстрирует возможность существенной чистой фиксации диоксида углерода и преобразования газообразного сырья в липиды для производства биодизельного топлива. Система может быть дополнительно оптимизирована, чтобы приблизиться к производительности ее отдельных агрегатов, чтобы ее можно было использовать для экономичного преобразования отходящих газов сталелитейных заводов в ценное жидкое топливо для транспортировки.
Система может быть дополнительно оптимизирована, чтобы приблизиться к производительности ее отдельных агрегатов, чтобы ее можно было использовать для экономичного преобразования отходящих газов сталелитейных заводов в ценное жидкое топливо для транспортировки.
Обеспокоенность сокращением запасов нефти и изменяющими климат выбросами парниковых газов привела к призывам к использованию чистых и возобновляемых жидких видов топлива (1). Одним из перспективных направлений является производство микробного масла из углеводного сырья. Это масло можно легко преобразовать в биодизельное топливо, и в последнее время был достигнут значительный прогресс в разработке маслянистых микробов для производства липидов из сахаров (2–5). Основной проблемой этого подхода была относительно высокая стоимость сахарного сырья.В качестве альтернативы были исследованы менее дорогие промышленные газы, содержащие CO 2 с восстановителями, такими как CO или H 2 . В одном применении анаэробный Clostridia использовался для преобразования синтез-газа в этанол (6), хотя и при низкой концентрации, требующей высокой стоимости разделения. Здесь мы представляем альтернативный подход «газ-липиды», который преодолевает недостатки предыдущих схем.
Здесь мы представляем альтернативный подход «газ-липиды», который преодолевает недостатки предыдущих схем.
Ранее нами было показано, что ацетат с концентрацией более 30 г / л может быть получен из смесей CO 2 и CO / H 2 с использованием эволюционированного штамма ацетогена Moorella thermoacetica со значительной производительностью 0.55 г⋅л −1 ⋅h −1 и выход 92% (7). Мы также продемонстрировали, что разработка масляных дрожжей Yarrowia lipolytica может давать биокатализаторы, которые могут производить липиды из глюкозы с высокими выходами и высокой продуктивностью (2, 5). В то же время, в рамках поиска недорогого сырья, мы исследовали производство липидов из других субстратов, таких как ацетат и другие летучие жирные кислоты (ЛЖК), которые потенциально могут быть получены с меньшими затратами как продукты анаэробного сбраживания или из выхлопных газов. в производстве стали.В этом исследовании мы показываем, что две вышеупомянутые системы могут быть объединены в двухступенчатый процесс, в котором CO 2 и CO / H 2 превращаются в уксусную кислоту в анаэробной барботажной колонке биореактора первой ступени, а продукт — уксусная кислота. кислота затем превращается в липиды под действием Y. lipolytica в аэробном биореакторе второй ступени. Чтобы оценить достоинства этого подхода, мы индивидуально оптимизировали ферментацию M. thermoacetica и Y. lipolytica с целью максимизировать выход и продуктивность ацетата и липидов, соответственно.Фильтр с половолоконной мембраной был развернут в анаэробном биореакторе, чтобы обеспечить непрерывное удаление продукта уксусной кислоты и рециркуляцию клеток M. thermoacetica в пузырьковую анаэробную колонку. Аналогичным образом, рециркуляция клеток также использовалась во втором биореакторе для разделения времени пребывания, необходимого для роста и липогенеза в клетках Y. lipolytica , от потребления уксусной кислоты и, следовательно, для развития плотной микробной культуры и высокой концентрации липидов в второй биореактор.Мы также впервые продемонстрировали, насколько нам известно, отделение фазы роста M. thermoacetica от фазы производства уксусной кислоты: сначала устойчивая культура M.
кислота затем превращается в липиды под действием Y. lipolytica в аэробном биореакторе второй ступени. Чтобы оценить достоинства этого подхода, мы индивидуально оптимизировали ферментацию M. thermoacetica и Y. lipolytica с целью максимизировать выход и продуктивность ацетата и липидов, соответственно.Фильтр с половолоконной мембраной был развернут в анаэробном биореакторе, чтобы обеспечить непрерывное удаление продукта уксусной кислоты и рециркуляцию клеток M. thermoacetica в пузырьковую анаэробную колонку. Аналогичным образом, рециркуляция клеток также использовалась во втором биореакторе для разделения времени пребывания, необходимого для роста и липогенеза в клетках Y. lipolytica , от потребления уксусной кислоты и, следовательно, для развития плотной микробной культуры и высокой концентрации липидов в второй биореактор.Мы также впервые продемонстрировали, насколько нам известно, отделение фазы роста M. thermoacetica от фазы производства уксусной кислоты: сначала устойчивая культура M. thermoacetica устанавливается в CO-зависимой фазе роста посредством с использованием газовой смеси CO 2 / CO, а затем состав газа переключается на смесь H 2 / CO 2 , которая дает ацетат со значительно более высокой удельной производительностью. Этот прогресс позволил нам обеспечить как высокую удельную производительность, так и высокую плотность ячеек М.thermoacetica для общей очень высокой объемной производительности 0,9 г ацетата ⋅L −1 h −1 . Затем эти два процесса объединяются в единую схему переработки газа в нефть с непрерывным потоком (рис. 1), при этом проектные решения основываются на рабочих характеристиках отдельных реакторов.
thermoacetica устанавливается в CO-зависимой фазе роста посредством с использованием газовой смеси CO 2 / CO, а затем состав газа переключается на смесь H 2 / CO 2 , которая дает ацетат со значительно более высокой удельной производительностью. Этот прогресс позволил нам обеспечить как высокую удельную производительность, так и высокую плотность ячеек М.thermoacetica для общей очень высокой объемной производительности 0,9 г ацетата ⋅L −1 h −1 . Затем эти два процесса объединяются в единую схему переработки газа в нефть с непрерывным потоком (рис. 1), при этом проектные решения основываются на рабочих характеристиках отдельных реакторов.
Рис. 1.
Интегрированный биопроцесс: Схема двухэтапного процесса производства липидов с использованием микробной конверсии. На стадии 1 CO 2 ферментируется до летучей жирной кислоты; на стадии 2 эта кислота превращается в липиды с помощью искусственного штамма.
Результаты
Рост клеток и производство ацетата из синтез-газа.
Производство уксусной кислоты из синтез-газа с помощью M. thermoacetica показано на рис. 2, на котором представлены зависимости от времени роста и титра уксусной кислоты в анаэробной барботажной колонке, работающей независимо. Наша предыдущая работа послужила основой для скоростей потока, относящихся к этому исследованию (7). Ферментация проводилась при скорости потока 1000 стандартных кубических сантиметров в минуту (sccm) с использованием CO или H 2 в качестве восстановительного газа в составе 7/3 CO / CO 2 или 7/3 H 2. / CO 2 .Значительные количества уксусной кислоты (более 30 г / л) были произведены в обоих условиях в течение аналогичных периодов времени. Примечательно, что максимальная плотность клеток при H 2 (макс. OD ~ 2,5) была менее четверти плотности, достигнутой с CO (макс. OD ~ 11) в качестве донора электронов. Поскольку объемные производительности уксусной кислоты в этих двух экспериментах были одинаковыми, удельная производительность уксусной кислоты при H 2 / CO 2 была в четыре раза больше, чем при CO / CO 2 .Эта разница в удельной продуктивности клеток, вероятно, связана с энергетической разницей между H 2 и метаболизмом CO в этом организме. M. thermoacetica генерирует АТФ в автотрофных условиях с помощью хемиосмоса. В этом механизме окисление восстановленного ферредоксина энергосберегающим гидрогеназным комплексом (Ech) приводит к перемещению протонов через мембрану. Генерируемый протонный градиент используется связанной с мембраной АТФ-синтазой для генерации АТФ (8). Производство ацетил-КоА из H 2 / CO 2 включает окисление 2 моль ферредоксина на каждый моль синтезированного ацетил-КоА, тогда как для получения ацетил-КоА из СО требуется окисление 6 моль ферредоксина.Таким образом, рост на CO поддерживает большее производство АТФ, что, в свою очередь, приводит к более высоким концентрациям биомассы.
Поскольку объемные производительности уксусной кислоты в этих двух экспериментах были одинаковыми, удельная производительность уксусной кислоты при H 2 / CO 2 была в четыре раза больше, чем при CO / CO 2 .Эта разница в удельной продуктивности клеток, вероятно, связана с энергетической разницей между H 2 и метаболизмом CO в этом организме. M. thermoacetica генерирует АТФ в автотрофных условиях с помощью хемиосмоса. В этом механизме окисление восстановленного ферредоксина энергосберегающим гидрогеназным комплексом (Ech) приводит к перемещению протонов через мембрану. Генерируемый протонный градиент используется связанной с мембраной АТФ-синтазой для генерации АТФ (8). Производство ацетил-КоА из H 2 / CO 2 включает окисление 2 моль ферредоксина на каждый моль синтезированного ацетил-КоА, тогда как для получения ацетил-КоА из СО требуется окисление 6 моль ферредоксина.Таким образом, рост на CO поддерживает большее производство АТФ, что, в свою очередь, приводит к более высоким концентрациям биомассы. Очевидное ограничение АТФ во время роста на H 2 / CO 2 заставляет увеличивать отвлечение ацетил-КоА от синтеза биомассы на производство ацетата для увеличения синтеза АТФ через фосфорилирование на уровне субстрата, что приводит к более высоким общим потокам ацетата на единицу биомассы.
Очевидное ограничение АТФ во время роста на H 2 / CO 2 заставляет увеличивать отвлечение ацетил-КоА от синтеза биомассы на производство ацетата для увеличения синтеза АТФ через фосфорилирование на уровне субстрата, что приводит к более высоким общим потокам ацетата на единицу биомассы.
Рис. 2.
Рост клеток и производство уксусной кислоты с использованием CO или H 2 в качестве восстановительного газа в составе 7/3 CO / CO 2 или 7/3 H 2 / CO 2 и расход 1000 кубических сантиметров в минуту.Максимальная плотность клеток при H 2 (макс. OD ~ 2,5) составляет менее одной четверти от плотности, достигаемой с CO (макс. OD ~ 11) в качестве донора электронов. Значительные количества уксусной кислоты (~ 30 г / л) производятся в обоих условиях. Представлены SD из трех прогонов.
Производительность ацетата с переключателем состава газа и заменой среды.
Как показано в предыдущем разделе, удельная производительность ацетата на H 2 на M. thermoacetica примерно в четыре раза выше, чем на CO.С другой стороны, гораздо более высокие плотности клеток могут поддерживаться смесью CO / CO 2 . Это говорит о том, что сначала следует вырастить культуру M. thermoacetica на смеси CO / CO 2 и переключиться на композицию H 2 / CO 2 после того, как культура будет создана, чтобы воспользоваться преимуществами более высокой специфичности к ацетату. производительность по водороду. Таким образом, был разработан эксперимент, чтобы оценить, можно ли использовать высокую плотность клеток, достигаемую при выращивании на CO / CO 2 , для повышения общей производительности путем переключения газового состава на H 2 / CO 2 после начальной фазы роста.Однако простое переключение состава газа привело к значительному снижению культуры M. thermoacetica и отсутствию изменений в продукции уксусной кислоты (рис. 3). Мы предположили, что это может быть связано с низкой активностью гидрогеназы во время переключения, которая, как известно, ингибируется монооксидом углерода (рис.
thermoacetica примерно в четыре раза выше, чем на CO.С другой стороны, гораздо более высокие плотности клеток могут поддерживаться смесью CO / CO 2 . Это говорит о том, что сначала следует вырастить культуру M. thermoacetica на смеси CO / CO 2 и переключиться на композицию H 2 / CO 2 после того, как культура будет создана, чтобы воспользоваться преимуществами более высокой специфичности к ацетату. производительность по водороду. Таким образом, был разработан эксперимент, чтобы оценить, можно ли использовать высокую плотность клеток, достигаемую при выращивании на CO / CO 2 , для повышения общей производительности путем переключения газового состава на H 2 / CO 2 после начальной фазы роста.Однако простое переключение состава газа привело к значительному снижению культуры M. thermoacetica и отсутствию изменений в продукции уксусной кислоты (рис. 3). Мы предположили, что это может быть связано с низкой активностью гидрогеназы во время переключения, которая, как известно, ингибируется монооксидом углерода (рис. 3 B ). Несмотря на то, что гидрогеназная активность экспрессируется конститутивно, активность гидрогеназы в 18 раз выше в клетках, культивируемых H 2 , чем в клетках, выращенных на CO (9), и она необходима для роста на H 2 в качестве единственного донора электронов.Успешный переход от CO к водороду без снижения клеточной массы, а также поддержание биосинтетической способности клеток был достигнут, когда половина среды была заменена свежей средой одновременно с переключением газа. В этом эксперименте после начального снижения, вызванного разбавлением из свежей среды, плотность клеток стабилизировалась (рис. 3 C ) на новом значении после переключения газа и, что более важно, сохранялась продуктивность уксусной кислоты. Средняя общая производительность по уксусной кислоте 0.9 г⋅л -1 ⋅ч -1 после переключения газа было получено, что на 50% выше, чем 0,6 г⋅л -1 ⋅ч -1 , наблюдаемое до переключения газа.
3 B ). Несмотря на то, что гидрогеназная активность экспрессируется конститутивно, активность гидрогеназы в 18 раз выше в клетках, культивируемых H 2 , чем в клетках, выращенных на CO (9), и она необходима для роста на H 2 в качестве единственного донора электронов.Успешный переход от CO к водороду без снижения клеточной массы, а также поддержание биосинтетической способности клеток был достигнут, когда половина среды была заменена свежей средой одновременно с переключением газа. В этом эксперименте после начального снижения, вызванного разбавлением из свежей среды, плотность клеток стабилизировалась (рис. 3 C ) на новом значении после переключения газа и, что более важно, сохранялась продуктивность уксусной кислоты. Средняя общая производительность по уксусной кислоте 0.9 г⋅л -1 ⋅ч -1 после переключения газа было получено, что на 50% выше, чем 0,6 г⋅л -1 ⋅ч -1 , наблюдаемое до переключения газа. Эти результаты согласуются с динамикой активности гидрогеназы, которая увеличилась примерно в 20 раз за 1 день после замены CO на H 2 . Этот эксперимент продемонстрировал, что объемная производительность уксусной кислоты может быть значительно улучшена путем изменения состава газа и замены среды в середине цикла по сравнению с тем, что было возможно до использования CO 2 / H 2 или только CO 2 / газ CO. .
Эти результаты согласуются с динамикой активности гидрогеназы, которая увеличилась примерно в 20 раз за 1 день после замены CO на H 2 . Этот эксперимент продемонстрировал, что объемная производительность уксусной кислоты может быть значительно улучшена путем изменения состава газа и замены среды в середине цикла по сравнению с тем, что было возможно до использования CO 2 / H 2 или только CO 2 / газ CO. .
Рис. 3.
( A – C ) Временные зависимости ( A ) концентрации уксусной кислоты, ( B ) удельной гидрогеназной активности и ( C ) оптической плотности для двух различных методов переключения газа состав в анаэробной пузырьковой колонке. Сплошные символы соответствуют случаю, когда было выполнено переключение газа с CO / CO 2 (4/1) и расхода 1000 sccm на H 2 / CO 2 (2/1) и то же самое. Скорость потока сопровождалась заменой половины реакционной среды свежей средой. В ходе, обозначенном открытыми символами, было выполнено аналогичное переключение газа, но без замены среды. Представлены SD из трех прогонов.
В ходе, обозначенном открытыми символами, было выполнено аналогичное переключение газа, но без замены среды. Представлены SD из трех прогонов.
Производство липидов из сильнодействующей уксусной кислоты с помощью
Y. lipolytica .
Производство липидов из уксусной кислоты (30% об. / Об.) Y. lipolytica в периодическом режиме с подпиткой показано на рис. 4. Y. lipolytica продуцировал липиды с титром 51 г / л с продуктивность 0,26 г 900л -1 ч -1 и содержание липидов 61%, что является самым высоким показателем для ацетата на сегодняшний день.Fontannile et al. (10) вырастили Y. lipolytica сначала на глюкозе, а затем перенесли на ЛЖК, получив более низкую продуктивность (0,16 г⋅л -1 ⋅ч -1 ) по сравнению с нашим исследованием, хотя и при более низких титрах липидов (12 г / Л), выход конверсии (0,13 г / г) и содержание липидов 40%.
Рис. 4.
Характеристики ферментации Y. lipolytica в полунепрерывном режиме при потреблении уксусной кислоты (высокой крепости). Y. lipolytica продуцировал липиды с титром 51 г / л с продуктивностью 0.26 г⋅л −1 ⋅h −1 и содержание липидов 61%. Представлены SD из трех прогонов.
Производство липидов из уксусной кислоты с низкой активностью с помощью
Y. lipolytica .
При разбавлении субстрата получается разбавленный продукт. Исключение возможно в случае внутриклеточных продуктов (например, липидов), а также когда клетки рециркулируют, чтобы увеличить время их пребывания в биореакторе, чтобы дать им больше времени для достижения более высокого содержания липидов. Этого можно достичь с помощью мембраны из полых волокон, при которой отработанная среда с низкой концентрацией остаточного ацетата удаляется, а клетки возвращаются обратно в биореактор.Эта схема была реализована, и на рис. 5 показаны временные зависимости производства липидов из разбавленной уксусной кислоты (3% об. / Об.). Титр липидов 46 г / л был получен при общей продуктивности 0,27 г⋅л -1 ч -1 и содержании липидов 59%. Средний профиль липидного состава, полученный в этом опыте, показан на рис. 6. Этот профиль аналогичен профилю Knothe (11), с более высокими фракциями ненасыщенных жиров, которые желательны, поскольку они увеличивают цетановое число и снижают точку помутнения полученный биодизель.
Рис. 5.
Расход уксусной кислоты (3% об. / Об.) (Низкая концентрация) и производство липидов при использовании Y. lipolytica в полунепрерывном режиме. Модуль из полых волокон использовался для рециркуляции ячеек и поддержания постоянного объема. Временные графики показывают титр липидов 46 г / л с общей продуктивностью 0,27 г⋅л -1 ⋅ч -1 и содержанием липидов 59%. Представлены SD из трех прогонов.
Рис. 6.
Распределение жирных кислот во время ферментации в биореакторе с использованием Y.lipolytica . Показаны пальмитат C16, пальмитолеат C16.1, стеарат C18, олеат C18.1 и линолеат C18.2. Образцы были выполнены в трех экземплярах.
Потоки углерода были рассчитаны для этого прогона. Y. lipolytica потребляет уксусную кислоту и превращает углерод в CO 2 , липиды и нелипидную биомассу с небольшими количествами цитрата, образующегося в качестве побочного продукта. Кумулятивный баланс массы углерода близок к 5%, при этом CO 2 составляет 54% от общего количества углеродных продуктов (рис.7). Была построена стехиометрическая модель для оценки эффективности использования ацетата в процессе ферментации с учетом обычных метаболических процессов и связанных с ними затрат АТФ и НАДФН для производства (роста) нелипидной биомассы, а также производства липидов. Подробная информация о модели приведена в Примечаниях SI к модели . Модель по существу предсказывает для данного количества образовавшихся липидов и биомассы необходимое количество ацетата и образовавшегося CO 2 , основываясь на разумных предположениях о путях, ответственных за основные метаболические процессы, лежащие в основе роста и синтеза липидов.Подставляя экспериментально измеренные данные о производстве липидов и нелипидов, мы определили теоретически предсказанное количество потребления ацетата и производства диоксида углерода. При сравнении с соответствующими экспериментально наблюдаемыми уровнями потребления ацетата и продукции CO 2 можно увидеть, что экспериментальная продукция липидов и продукция нелипидов находятся в пределах 10% от теоретических значений, как показано на рис. 8. Это говорит о том, что сконструированный штамм хорошо оптимизирован для синтеза липидов, тратя очень мало субстрата на другие процессы.
Рис. 7.
Углеродный баланс потребления ацетата и производства липидов. Показаны входящий углерод в виде ацетата и выходной углерод (липидный, нелипидный, побочные продукты и CO 2 ). Кумулятивный баланс массы углерода близок к 5%, при этом CO 2 составляет 54% от общего количества углеродных продуктов.
Рис. 8.
Теоретические прогнозы и экспериментальные значения израсходованного ацетата и произведенного CO 2 . Для оценки эффективности использования ацетата в процессе ферментации была построена стехиометрическая модель с учетом потребленного ацетата и производимого CO 2 как для производства нелипидной биомассы (роста), так и для производства липидов, включая связанные с этим затраты на АТФ и НАДФН. .Экспериментальное производство CO 2 и расход ацетата находятся в пределах 10% от ожидаемых теоретических значений. Подробная информация о модели приведена в Примечаниях SI к модели .
Интегрированная система биоконверсии синтез-газа в липиды.
На основе результатов, полученных с двумя блоками биореактора, интегрированная система, показанная на рис. 1, была собрана и работала, как показано в таблице 1. На рис. 9 показаны временные зависимости роста клеток и производства уксусной кислоты с помощью M. thermoacetica в анаэробной пузырьковой колонке с рис.10 резюмируя то же самое для Y. lipolytica в аэробном биореакторе с мешалкой. Перед 93 часами (первая фаза) в анаэробный биореактор подавали газовую смесь CO / CO 2 при 1000 см3 / мин и составом (4/1). В течение этого периода, M. thermoacetica выросла до OD 10,3, а уксусная кислота накапливалась до 12 г / л с производительностью 0,4 г⋅л -1 ⋅h -1 , исключая лаг-фазу. Затем подачу газа изменили на H 2 / CO 2 с расходом 1200 куб. См / см и составом (2/1).Вторая фаза длилась от 93 часов до 218 часов и характеризовалась постоянным увеличением содержания уксусной кислоты до достижения максимума 25 г / л. После переключения газа OD ячейки упал с максимального значения 10,3 до примерно 8 и медленно восстанавливался до конца второй фазы (см. Рис. S1 для различных соотношений сред). В то же время (186–218 ч) из анаэробного биореактора через половолоконную мембрану удаляли около 1000 мл жидкой среды и подавали в аэробный биореактор. На третьей фазе (через 218 ч) была инициирована работа в непрерывном режиме, при которой уровень уксусной кислоты в анаэробном реакторе поддерживался на уровне максимальной концентрации ~ 25 г / л.Это было достигнуто путем непрерывного удаления уксусной кислоты при рециркуляции клеток M. thermoacetica через мембрану из полых волокон. Рост клеток во время этой фазы был минимальным, и реактор, таким образом, работал как перфузионный биореактор. Максимальная концентрация уксусной кислоты 25 г / л была выбрана для предотвращения ингибирования дальнейшего образования ацетата (7). Рабочие объемы обоих биореакторов поддерживались постоянными путем добавления свежей среды в первый биореактор и удаления отработанной среды из аэробного биореактора, как показано на рис.1. Концентрация уксусной кислоты в резервуаре для среды измерялась периодически между 118 часами и 312 часами, всего за 194 часа было произведено 212 г уксусной кислоты. Средняя производительность по уксусной кислоте составила 1,1 г⋅л -1 ⋅ч -1 после переключения газа, что в три раза выше, чем на первой стадии, когда в качестве газового сырья использовался CO / CO 2 .
Таблица 1.
Условия эксперимента во время интегрированного биопроцесса
Рис. 9.
Рост клеток M. thermoacetica и производство уксусной кислоты в интегрированном эксперименте по ферментации.Во всех трех фазах газообразный субстрат предоставляется в непрерывном режиме, тогда как жидкий в периодическом режиме предоставляется в первых двух фазах. В третьей фазе и газ, и жидкость находятся в непрерывном режиме. Успешное переключение на газообразный субстрат позволило получить уксусную кислоту (максимальная концентрация ~ 25 г / л) в анаэробном реакторе. Это достигается путем непрерывного удаления уксусной кислоты при рециркуляции клеток M. thermoacetica через мембрану из полых волокон. Представлены SD из трех прогонов.
Рис. 10.
Титр липидов и производство биомассы в интегрированном процессе (фаза III). Показана динамика роста клеток и продукции липидов (титр 18 г / л и содержание липидов 36%) в аэробном биореакторе. Представлены SD из трех прогонов.
Рис. S1.
Динамика концентрации и оптической плотности уксусной кислоты для различных соотношений замещения среды при изменении состава газа в анаэробной барботажной колонке. Оценивали три различных коэффициента замены среды (50%, 75% и 90%).Все опыты показали сходные закономерности: производство возобновлялось после задержки примерно на 1 или 2 дня, и производство прекращалось при концентрации уксусной кислоты около 25–30 г / л.
Динамика роста клеток и продукции липидов в аэробном биореакторе представлена на рис. 10. Титр липидов составлял 18 г / л, а содержание липидов — 36%. Хотя эти цифры ниже, чем полученные в отдельных единицах и в предыдущих исследованиях (2), результаты, тем не менее, обнадеживают, поскольку они демонстрируют осуществимость интегрированного процесса превращения газа в липиды, что было целью данного исследования.Сравнение результатов, полученных для одноступенчатых биореакторов и результатов комбинированного процесса, представлено в таблице 2. Основное различие между независимым циклом получения липидов и интегрированным процессом заключается в выходе липидов из уксусной кислоты. В одном исследовании больше уксусной кислоты было преобразовано в липиды, тогда как в комбинированном процессе больше уксусной кислоты было преобразовано в нелипидную биомассу. Известно, что в Y. lipolytica соотношение C / N сильно влияет на продукцию липидов и титры.В комбинированном процессе соотношение C / N строго не контролировалось, и это, вероятно, отрицательно повлияло на урожайность. Следовательно, будущие эксперименты должны быть направлены на минимизацию содержания азота в среде M. thermoacetica , что ограничит содержание азота в исходной уксусной кислоте, подаваемой в реактор Y. lipolytica после начала фазы производства липидов.
Таблица 2.
Сравнение результатов одностадийных и интегрированных процессов
SI Примечания к модели
Обзор.
Теоретический максимум накопления углерода в липидах рассчитывается на основе микробного метаболизма для определения стехиометрии липидного и нелипидного образования ацетата. Цель этого расчета — определить эффективность маслянистого микроба в превращении ацетата в липиды в процессе ферментации. Теперь, чтобы микроб накапливал липиды, он должен сначала произвести нелипидную биомассу из ацетата, а затем отвести последующий углерод в сторону накопления липидов. Таким образом, ацетат, потребляемый микробами, будет направлен на один из двух конечных продуктов: нелипидную биомассу и липиды.Таким образом, мы пытаемся выяснить, потребляет ли микроб больше, чем теоретически необходимое количество ацетата (углеродное сырье), или производит ли он больше, чем теоретически необходимое количество диоксида углерода (потерянный углерод), чтобы производить наблюдаемое количество липидов и нелипидов во время ферментация. С этой целью мы сначала разработали модель, которая описывает стехиометрию превращения уксусной кислоты в соответствующий продукт.
Производство липидов на уксусной кислоте.
Стехиометрия производства липидов из уксусной кислоты была получена путем учета (–) уксусной кислоты, необходимой для производства трипальмитина (наша модель липида, триглицеридной формы пальмитиновой кислоты), ( ii ) уксусной кислоты, необходимой для производства НАДФН. (уменьшающий эквивалент) для поддержания производства липидов и ( iii ) уксусная кислота, необходимая для производства АТФ для поддержания производства липидов.Окончательное уравнение, связывающее уксусную кислоту с образованием липидов: 50,1 Ch4COOH → 49,2 CO2 + C51H98O6. [S1] Вышеприведенное уравнение дает теоретические количества необходимой уксусной кислоты и диоксида углерода, образующегося при производстве 1 моля трипальмитина. Подробная информация о его происхождении представлена в SI Notes on the Model , Stoichiometry for Acetate Conversion to Lipids . Используя это уравнение и молекулярные массы ацетата и трипальмитина, мы вычисляем максимальный теоретический выход производства липидов из ацетата при 0.272 г липидов на грамм ацетата.
Производство нелипидной биомассы на ацетате.
Аналогичным образом была разработана модель производства нелипидной биомассы из ацетата, которая учитывает ( и ) химическую формулу нелипидной биомассы, ( ii ) теоретическую массу сухих клеток, производимых на электрон, и (). iii ) ацетат, израсходованный на производство АТФ. Окончательное уравнение: 6.3 Ch4COOH → 7.7 CO2 + C5H8.3O2.7N0.7. [S2] Таким образом, мы получили стехиометрическое уравнение, которое связывает производство нелипидной биомассы с количеством израсходованных молей ацетата и молей произведенного CO 2 .Путем включения наблюдаемых измерений липидных и нелипидных количеств в уравнения. S1 и S2 соответственно, можно получить теоретические уровни потребления уксусной кислоты и производства диоксида углерода, связанные с каждым преобразованием. Теоретические оценки потребляемой уксусной кислоты и продуцируемого диоксида углерода сравниваются в тексте с наблюдаемыми экспериментальными количествами на рис. 8, чтобы определить степень неэффективности микробного метаболизма во время ферментации.
Подробная информация о моделях.
Стехиометрия превращения ацетата в липиды.
Биосинтез триглицеридов из ацетата требует нескольких путей. Глюконеогенез в конечном итоге обеспечивает основу глицерина. Поскольку исходным субстратом для глюконеогенеза является четырехуглеродное соединение (оксалоацетат / пируват), требуются анаплеротические пути, такие как глиоксалатный цикл или метилцитратный цикл, когда ацетат является субстратом. Биосинтез жирных кислот катализирует АТФ- и НАДФН-зависимое превращение ацетата в пальмитиновую кислоту, и, наконец, путь Кеннеди конденсирует глицерин с липидами с образованием триглицеридов.Все вышеперечисленные пути, а также пути образования НАДФН и АТФ принимаются во внимание, чтобы прийти к окончательному уравнению отношения ацетата к липидам. Обратите внимание, что уравнение образования АТФ также используется для прогнозирования стехиометрии биомассы в SI Notes on the Model , Stoichiometry for Acetate Conversion to Nonlipid Biomass .
Реакции, участвующие в этом процессе, для простоты сгруппированы в модули или наборы. Символы (c) и (m) указывают, существует ли метаболит в цитозоле или в митохондриях.Были приняты следующие модули реакций: ( i ) ацетат в ацетил-КоА (ACA), ( ii ) ACA в оксалоацетат (OAA), ( iii ) OAA в глицерин, ( iv ) ACA в C16-жирная кислота и ( v ) (жирная кислота + глицерин) образует липид.
Проанализируем уравнения каждого из вышеперечисленных модулей.
Набор i.
Ацетат + АТФ → Ацетил-КоА (ацетил-КоА-синтетаза). [S3] Эта реакция протекает под действием фермента ацетил-КоА-синтетазы (ACS) в цитозоле.
Набор ii.
Глюконеогенез происходит в цитозоле, и, следовательно, оксалоацетат должен присутствовать на стороне цитозоля, чтобы инициировать глюконеогенез. Этот процесс происходит через ряд последовательных реакций. Во-первых, работает глиоксалатный цикл, и на каждые две молекулы ацетил-КоА образуется сукцинат. Затем сукцинат, продуцируемый в цитозоле, проникает через митохондриальную мембрану и входит в цикл TCA, действующий в митохондриях. Сукцинат превращается в малат, который проникает в цитозоль.На цитозольный малат воздействует яблочный фермент с образованием пирувата, на который в конечном итоге воздействует фермент пируваткарбоксилаза с образованием оксалоацетата в цитозоле. Реакции следующие:
. 2 ACA (c) → сукцинат (c) + NADHc (глиоксалатный цикл) (28)
. Сукцинат (c) → сукцинат (m) (выход сукцината)
. Сукцинат (m) → малат (m) + FADH 2 (цикл TCA) (28)
. Малат (m) → малат (c) (выход малата)
.Малат (c) → пируват (c) + NADPHc + CO 2 (яблочный фермент) (28)
. Пируват (c) + CO 2 + ATP → OAA (c) (пируваткарбоксилаза) (28)
Суммарная реакция составляет 2 ACA (c) + ATP → OAA (c) + NADHc + FADh3 + NADPHc. [S4]
Набор iii.
Это составляет сумму реакций, ведущих к производству глицерина из оксалоацетата посредством глюконеогенеза (28): OAA (c) + GTP + ATP + NADHc → Glycerol + CO2 (глюконеогенез). [S5]
Set iv.
Это объясняет набор реакций, ведущих к производству пальмитиновой кислоты из ацетил-КоА по пути синтеза жирных кислот (29): 24 ACA (c) + 18 NADPH + 24 NADHc + 69 ATP → 3 пальмитиновая кислота (синтез жирных кислот ). [S6]
Set v.
Это учитывает производство трипальмитина по пути Кеннеди (28): глицерин (c) +3 пальмитиновая кислота + АТФ → трипальмитин (путь Кеннеди). [S7] После того, как реакционные модули были проанализированы для получения единственной реакции, следующий шаг включает их сложение для получения окончательного уравнения.Добавление наборов ii – v (реакции 2–5) даст следующие уравнения: 2 ACA (c) + ATP → OAA (c) + NADHc + FADh3 + NADPHc [S4] OAA (c) + GTP + ATP + NADHc → глицерин + CO2 (глюконеогенез) [S5] 24 ACA (c) +18 NADPH + 24 NADHc + 69 ATP → 3 пальмитиновая кислота (синтез жирных кислот) [S6] Глицерин (c) +3 пальмитиновая кислота + ATP → трипальмитин (Кеннеди путь) [S7] с чистыми уравнениями: 26 ACA (c) +17 NADPHc + 72 ATP + GTP + 24 NADHc → трипальмитин + CO2 + FADh3. [S8] На этом этапе ацетат, необходимый для обеспечения необходимого NADPH, NADH, и необходимо учитывать АТФ.
Мы предполагаем, что весь НАДФН обеспечивается действием яблочного фермента. Следующее уравнение учитывает производство НАДФН: НАДНс + АТФ → НАДФНс (яблочный фермент). [S9] Производство АТФ из цитозольного АСА не так просто, поскольку АКА не может пересечь митохондриальную мембрану с образованием митохондриального АКА, который затем может напрямую войти в цикл TCA . Таким образом, глиоксалатный цикл образует сукцинат, который в конечном итоге образует пируват. Пируват может проникать через митохондрии, а затем декарбоксилатировать с образованием ацетил-КоА, который впоследствии входит в цикл TCA.Уравнение для производства АТФ / НАДН через цикл TCA из цитозольного ацетил-КоА выполняется с помощью следующей системы уравнений:
. 2 ACA (c) → сукцинат (c) + NADHc (глиоксалатный цикл)
. Сукцинат (c) → сукцинат (m) (выход сукцината)
. Сукцинат (m) → малат (m) + FADH 2 (цикл TCA)
. Малат (m) → малат (c) (выход малата)
. Малат (c) → пируват (c) + NADPHc + CO 2 (яблочный фермент) (28)
.Пируват (c) → пируват (m) (выход пирувата)
. Пируват (м) → 3 CO 2 + 4 NADHm + FADH 2 + GTP (цикл TCA) (28)
. 4 NADHm → 4 NADHc (29)
Чистое уравнение: 2 ACA (c) → 4 CO2 + 5 NADHc + 2 FADh3 + GTP + NADPHc. [S10] Уравнение. S10 также можно использовать для производства большего количества АТФ за счет превращения NADH и FADH 2 в цепи переноса электронов. Однако мы также предполагаем, что NADPH не будет окисляться, потому что существует высокая потребность в NADPH в клетке во время синтеза жирных кислот в качестве восстанавливающего агента (1 NADH = 2.5 АТФ, 1 ФАДН 2 = 1,5 АТФ, 1 ГТФ = 1 АТФ).
Уравнение будет выглядеть следующим образом: 2 ACA (c) → 4 CO2 + 16,5 ATP + NADPHc. [S11] Eqs. S8 — S11 складывается вместе, чтобы прийти к окончательному уравнению для производства липидов из ацетата. Используемая стратегия состоит в том, чтобы принять уравнения. S9 — S11 умножаются на неизвестные x, y и z и добавляются к уравнению. S8 . Уравнения добавляются таким образом, чтобы коэффициенты НАДН, НАДФН и АТФ в сумме равнялись 0. Таким образом, мы можем гарантировать, что уравнение учитывает только точное количество ацетата, необходимое для получения 1 моль трипальмитина: 26 АСА ( в) +17 NADPHc + 72 ATP + 1GTP + 24 NADHc → Трипальмитин + CO2 + FADh3.[S8] xNADHc + x ATP → xNADPHc — Умножение [ S9 ] на неизвестное x, 2y ACA (c) → 4y CO2 + 5y NADHc + 2y FADh3 + y GTP + y NADPHc. Умножение [ S10 ] на неизвестно y, 2z ACA (c) → 4z CO2 + 16,5z ATP + zNADPHc. Умножая [ S11 ] на неизвестное z, они складывают (26 + 2y + 2z) ACA + (17 − x − y − z) НАДФН + (71,5 + x − 4y − 16,5z) ATP + (24 + x − 5y) NADH → (4y + 4z + 1) CO2 + трипальмитин (превращающий FADh3 и GTP в АТФ). [S12] Однако субстратом является ацетат и, следовательно, умножая уравнение. S3 по (26 + 2y + 2z) и добавление к [ S12 ] заменит весь ACA ацетатом: (26 + 2y + 2z) ацетат + (17 − x − y − z) NADPH + (71.5 + x − 4y − 16,5z + 26 + 2y + 2z) ATP + (24 + x − 5y) NADH → (4y + 4z + 1) CO2 + трипальмитин. [S13] Присвоение коэффициентов NADPH, NADH и ATP к равным 0, мы получаем систему трех уравнений относительно x, y и z: 17 − x − y − z = 0 − коэффициент при NADPh34 + x − 5y = 0 − коэффициент при NADH97,5 + x − 2y − 14,5z. = 0 — коэффициент ATP. Решая три вышеупомянутых уравнения, мы получаем x = 4,944, y = 5,788 и z = 6,267.
Подставляя указанные выше значения x, y и z в уравнение. S13 , мы получаем окончательное уравнение для превращения ацетата в липиды как: 50.11 ацетат → 49,22 CO2 + трипальмитин (уравнение S1).
Стехиометрия конверсии ацетата в нелипидную биомассу.
Нелипидная биомасса средних дрожжей имеет химическую формулу C 5 H 8,3 O 2,7 N 0,7 (21). Это соответствует молекулярной массе 121,3 г / моль. Шулер и Карги (30) дали оценку выхода массы сухой ячейки (DCW) на один доступный электрон: 3,14 г DCW на электрон. Поскольку уксусная кислота имеет восемь электронов, это соответствует выходу биомассы (нелипидного), равному 3.14 × 8 = 25,1 г DCW на моль уксусной кислоты. При известной молекулярной массе средней биомассы дрожжей преобразование может быть показано как Ch4COOH → 0,21 C5H8,3O2,7N0,7 + 0,95 CO2. [S14] Здесь моли CO 2 были получены путем вычитания молей углерода в биомассе из количество молей углерода в уксусной кислоте (= 2 — 0,21 × 5).
Кроме того, клетка будет расходовать АТФ на производство биомассы. Согласно Verduyn (31), на грамм сухой биомассы требуется 105,5 ммоль АТФ, что означает, что на каждые 0.Произведено 21 моль биомассы, потребуется 2,65 моль АТФ.
Таким образом, уравнение. S14 будет изменен как Ch4COOH + 2,65 АТФ → 0,21 C5H8,3O2,7N0,7 + 0,95 CO2. [S15] Учет дополнительной уксусной кислоты, необходимой для производства 2,65 моль АТФ (описан в примечаниях SI к модели , Стехиометрия превращения ацетата в липиды ) и нормировав уравнение на 1 моль биомассы, мы получаем 6,3 Ch4COOH → 7,7 CO2 + C5H8,3O2,7N0,7 (уравнение S2).
Обсуждение
В этом исследовании было задействовано несколько новых концепций, которые позволили успешно реализовать интегрированный процесс преобразования газа в липиды.Во-первых, мы использовали acetogen M. thermoacetica в качестве модельного организма из-за его очень высокого автотрофного потока к ацетил-КоА, который естественным образом продуцирует ацетат с очень высокими скоростями и почти теоретическими выходами по каноническому пути Вуда – Люнгдаля. Кроме того, высокая рабочая температура ( T opt 60 ° C) этого термофильного организма делает его промышленным интересом, поскольку он требует меньшего охлаждения синтез-газа перед подачей в биореактор (12) по сравнению с ацетогенами других моделей, Clostridium ljungdahlii ( T opt 37 ° C) (13) и Acetobacterium woodii ( T opt 30 ° C) (14).Наша предыдущая работа с M. thermoacetica (7) обеспечила основу для получения уксусной кислоты с высокими скоростями, соответствующими данному исследованию.
Во-вторых, эта работа выдвигает на первый план новую стратегию переключения состава газа как важную часть процесса, необходимого для достижения более высокой общей производительности ацетата. Кроме того, этот результат указывает на важность физиологического состояния M. thermoacetica во время переключения газового состава, поэтому будущие эксперименты должны быть направлены на определение оптимальной замены среды и жизнеспособности культуры или альтернативного изменения состава среды для достижения максимальных титров. урожайность и продуктивность.
В-третьих, как показано в Таблице 2, показатели качества, полученные для интегрированной системы, ниже, чем для отдельных биореакторных единиц. Кроме того, общая энергетическая эффективность (от водорода до липидов и дрожжей) интегрированной системы составляет 34,4% по сравнению с максимальными теоретическими значениями 43% (с учетом содержания энергии в дрожжах) и 60,5% (при условии, что энергоносителями являются только водород и трипальмитин). . Подробная информация о модели расчета энергоэффективности приведена в Примечаниях к расчетам SI .Следовательно, процесс требует дальнейшей оптимизации. Контроль азота в среде двух установок упоминается как одно направление, которое может быть достигнуто с этой целью.
В-четвертых, существует значительный потенциал для снижения выбросов CO 2 в нашей системе по сравнению с одноступенчатыми системами. Например, теоретически ожидается, что процесс в первом реакторе будет потреблять 100,2 моль CO 2 , тогда как теоретически ожидается, что при аэробном синтезе липидов будет получено 49,22 моль CO 2 (совокупный баланс для всей операции).Таким образом, наш процесс фактически фиксирует CO 2 с использованием CO и / или H 2 в качестве восстановителей. Углекислый газ, образующийся в аэробном реакторе, производящем липиды, может быть переработан и использован анаэробными бактериями первой стадии, обеспечивая значительную общую скорость фиксации CO 2 . Точно так же нелипидную биомассу можно использовать для подачи дрожжевого экстракта, используемого в среде обоих реакторов после экстракции липидов.
Основным ограничением производства биодизеля (основной возобновляемой альтернативы дизельному топливу) является доступность и стоимость сырья (15).Маловероятно, что сырье, конкурирующее с пищевыми продуктами, внесет значительный вклад в производство возобновляемого транспортного топлива (16). В поисках более дешевого сырья синтез-газ предлагает привлекательные характеристики. Кроме того, в качестве экономичного сырья можно использовать сталеплавильный газ и природный газ (12, 17⇓ – 19). Таким образом, процесс преобразования синтез-газа в жидкости представляет собой платформу, совместимую с инфраструктурой, которая будет иметь важное значение для снижения зависимости от ископаемого топлива. Представленная здесь концепция преобразования газа в жидкость может обеспечить производство биодизеля из CO 2 таким образом, чтобы не предъявлять требований или изменений в землепользовании и не ограничиваться необходимостью доступа к углеводородному сырью.
SI Примечания по расчетам энергоэффективности
Экспериментальная энергоэффективность с использованием более низкой теплотворной способности.
Нижняя теплотворная способность (НТС): 120,21 МДж / кг водорода; 36,48 МДж / кг трипальмитина; 15,7 МДж / кг дрожжей
Энергоэффективность = (18 × 36,48 + 15,7 × 32) / (28 × 120,21) = 34,4%.
Теоретическая максимальная энергоэффективность. Рассмотрение только липидов в качестве продукта.
Водород LHV: -242,82 кДж / моль (cta.ornl.gov/bedb/appendix_a/Lower_and_Higher_Heating_Values_of_Gas_Liquid_and_Solid_Fuels.pdf).
Теплота сгорания трипальмитина: −31606 кДж / моль (webbook.nist.gov/cgi/cbook.cgi?ID=C555442&Mask=2).
Теплота сгорания по NIST является высшей теплотворной способностью (HHV). Чтобы преобразовать теплоту сгорания в LHV, необходимо учитывать теплоту парообразования: Жидкая вода: ΔfH ° жидкость = -285,83 кДж / моль Газообразная вода: ΔfH ° газ = −241,83 кДж / моль Вода: ΔfH ° = −241,83 — (- 285,83) = 44 кДж / моль; h3O (жидкость) h3O (г) (это 44 используется ниже) .HHV трипальмитина: ΔcH ° жидкость = -31,606 кДж / моль C51H98O6; C51H98O6 + 72,5 O2 → 51 CO2 + 49 h3O (1).LHV трипальмитина: ΔcH ° жидкость = -31,606 + (44) × (49 h3O) = -29,450 кДж / моль C51H98O6; C51H98O6 + 72,5 O2 → 51 CO2 + 49 h3O (г). Итак, теперь у нас LHV водорода: -242,82 кДж / мольТрипальмитин LHV: -29,450 кДж / моль.
Абсолютный максимум (без образования биомассы): 50,1 × [4 ч3 + 2 CO2 => ацетат] 50,1 ацетат => трипальмитин —————— 50,1 × 4 водорода = > трипальмитин Абсолютная максимальная (стехиометрическая) энергоэффективность: (−29,450 × 1 трипальмитин) / (- 242,82 × 50,1 × 4 водорода) = 60,5%.
Теоретическая максимальная энергоэффективность при обработке липидной и дрожжевой биомассы как продукта.
Используя экспериментальное соотношение продуцируемых липидов к биомассе, 50,11 ацетат => 49,22 CO2 + трипальмитин 50,11 × [4 ч3 + 2 CO2 => ацетат] —————— —- 50,11 × 4 водорода => трипальмитин (807,34 кг / кмоль) 6,3 ацетат => 7,7 CO2 + C5H8.3O2,7N0,76,3 × [4 ч3 + 2 CO2 => ацетат] ——— —————- 6,3 × 4 водорода => C5H8,3O2,7N0,7 (121,42 кг / кмоль) Экспериментально: биомасса = 32 г = 264 ммоль, липиды = 18 г = 22,3 ммоль. .
Итак, экспериментальное уравнение (где водород теоретически рассчитывается из приведенных выше теоретических уравнений и количества произведенных биомассы и липидов) 11,123 водорода => 264 C5H8.3O2,7N0,7 + 22,3 трипальмитин. Следовательно, теоретическая энергоэффективность (LHV) составляет [(264 моль био) (- 1 909,2524 кДж / моль) + (22,3 моль трип) (- 29 450 кДж / моль)] / [- (242,82 кДж) / моль) (11,123 моль ч3)] = 43%.
Материалы и методы
Бактерии, среды и условия культивирования.
Подробную информацию о повседневном культивировании микроорганизмов и описание используемых штаммов см. В SI Notes on Materials and Methods .
Анаэробный биореактор с пузырьковой колонкой.
М.thermoacetica выращивали в биореакторе на стеклянной барботажной колонке объемом 1 л при 60 ° C. Состав газа контролировали с помощью четырехканального регулятора массового расхода, а pH регулировали добавлением 5 н. Гидроксида натрия или соляной кислоты. Приготовленную среду (за исключением цистеина) автоклавировали, переносили в биореактор и продували бескислородным газом N 2 в течение ночи. pH доводили до 6,0, если не указано иное, и инициировали поток синтез-газа, который непрерывно барботировал через биореактор (см. SI Notes on Materials and Methods для получения информации о составе синтез-газа).К среде добавляли раствор цистеина для удаления остаточного кислорода, и биореактор инокулировали при 5% об. / Об.
Условия аэробного биореактора в резервуаре с перемешиванием.
Y. lipolytica выращивали в 2-литровом биореакторе с мешалкой. Растворенный кислород (DO) регулировали до 20% насыщения, а pH регулировали до 7,3 путем добавления уксусной кислоты. В течение первых 70 часов роста корм содержал 3% уксусной кислоты и 15 г / л сульфата аммония, чтобы обеспечить достаточное количество азота для образования нелипидной биомассы.После этого сырье содержало только 3% об. / Об. Уксусной кислоты. Дополнительный ацетат, необходимый для поддержания концентрации ацетата ~ 15 г / л, был предоставлен в виде раствора ацетата натрия (300 г / л). Модуль из полых волокон использовался для рециркуляции ячеек и поддержания постоянного объема (20). Теоретический максимум накопления углерода определяется как образование липидов и нелипидов на ацетате (21, 22).
Интегрированная система биопроцессов.
Биореактор с барботажной колонкой (для M. thermoacetica ) и биореактор с мешалкой (для Y.lipolytica ) были интегрированы в процесс, схематически показанный на фиг. 1. Условия эксперимента во время интегрированного биопроцесса представлены в таблице 1, а полная операция описана в SI Notes on Materials and Methods . Вкратце, барботажная колонна сначала работала в периодическом режиме по отношению к жидкой фазе. После изменения состава синтез-газа и достижения стационарной фазы было начато непрерывное удаление жидкости, и клетки были рециркулированы через половолоконную мембрану.После того, как был перенесен 1 л эффлюента, аэробный биореактор был инокулирован и работал непрерывно, снова с рециркуляцией клеток, осуществляемой через половолоконную мембрану.
Аналитика ферментации.
Состав отходящих газов анализировали с помощью microGC-TCD (газовая хроматография – детектор теплопроводности). Ацетат и цитрат измеряли с помощью ВЭЖХ с детектором показателя преломления (RID). Рост контролировали с помощью OD 600 для M. thermoacetica (23) и гравиметрически для Y.липолитика. Преобразование OD в сухой вес клеток осуществляли с помощью соотношений, определенных в нашей лаборатории. Количество общих липидов определяли с использованием модифицированной версии протокола прямой переэтерификации, адаптированной из патента США 7932077 (24) и Griffiths et al. (25) с использованием газовой хроматографии с пламенно-ионизационным детектором (GC-FID). Подробнее см. SI Примечания к материалам и методам .
Анализ гидрогеназы.
Активность гидрогеназы анализировали анаэробно по стандартным протоколам после восстановления бензилвиологена проницаемыми клетками в запечатанной кювете (26, 27).Подробнее см. SI Примечания к материалам и методам .
SI Примечания к материалам и методам
Бактерии, среды и условия культивирования.
Анаэробная ацетогенная бактерия M. thermoacetica (ATCC 49707) (www.atcc.org) была выращена при 60 ° C, следуя строгим аноксическим методикам, в улучшенной культуральной среде, содержащей (на литр) 1,4 г KH 2 PO 4 , 1,1 г K 2 HPO 4 , 2,0 г (NH 4 ) 2 SO 4 , 0.5 г MgSO 4 · 7H 2 O, 10 г дрожжевого экстракта, 10 г морфолиноэтансульфоновой кислоты (Mes), 20 мл раствора микроэлементов ATCC 1754 PETC (www.atcc.org) и 10 мл 0,3% раствора цистеина. Кроме того, добавляли 0,5 мл 0,2% резазурина, чтобы указать на присутствие кислорода.
Сконструированный штамм Y. lipolytica ACC-DGA (2) представляет собой po1g (генотип MatA, leu2-270, ura3-302: URA3, xpr2-332, axp-2; источник, Yeastern Biotech), трансформированный штамм с плазмида pMT065, экспрессирующая гены ACC и DGA, кодирующие ацетил-CoA-карбоксилазу и диацилглицерин-ацилтрансферазу, соответственно.ACC1 и DGA1 — важные гены, ответственные за первый и последний этапы синтеза липидов. Сочетание ACC1 и DGA1 позволяет эффективно отклонять поток в сторону синтеза липидов и создавать движущую силу (одновременное толкание и притяжение потока углерода в направлении TAG) путем связывания образования продукта в липидных телах. Этот штамм содержит маркер LEU2 и дополнительную копию генов ACC1 и DGA1. ACC1 находится под контролем промотора hp4d (минимальный промотор LEU2, которому предшествуют 4 копии энхансера вышестоящей последовательности активации UAS1B), а ген DGA1 находится под контролем промотора Yarrowia TEF [фактор элонгации транскрипции 1 (альфа)] с его ассоциированный интрон.
Сконструированный штамм Y. lipolytica ACC-DGA выращивали в следующих средах. Чашки селективного агара YNB-Leu содержали (на литр) 1,7 г дрожжевого азотного основания (без аминокислот), 0,69 г CSM (Leu-), 20 г глюкозы и 15 г агара Bacto. Среду YPD готовили (на литр) с 20 г бакто-пептона, 10 г дрожжевого экстракта и 20 г глюкозы (Sigma-Aldrich). Среда YPA была подобна YPD, но содержала 28 г / л ацетата натрия (или 20 г / л ацетата) вместо глюкозы. Посевной материал биореактора сначала выращивали в пробирке в течение ночи со средой YPD до OD 3–5 с последующим нанесением штрихов на чашку Петри YNB-Leu.Отдельные колонии пересевали в культуральную пробирку [3 мл YPA в культуральной пробирке на 15 мл, 200 об / мин, 28 ° C, 24 ч (орбитальный шейкер Thermo Scientific MaxQ 4000 с орбитой 1,9 см)]. Когда ОП достигала 3–5, их снова пересевали в колбу Эрленмейера при исходной ОП 0,1 [50 мл YPA в колбах на 250 мл, 200 об / мин, 28 ° C, 2 дня (орбитальный шейкер Thermo Scientific MaxQ 4000 с орбита 1,9 см)]. Биореактор инокулировали экспоненциально растущими клетками до конечной концентрации 5% об. / Об.Дрожжевой экстракт, бакто-агар и бакто-пептон были приобретены у BD. Ацетат натрия был приобретен у Macron Fine Chemicals. Все остальные используемые химические вещества были приобретены у Sigma-Aldrich. Штамм ACCDGA накапливал до 62% липидов из глюкозы в качестве субстрата в результате синтеза de novo при общей объемной производительности 0,143 г⋅л -1 ⋅h -1 (5). Последующие оптимизированные культивирования в биореакторе улучшили производительность до титра 55 г / л, 0,707 г⋅л -1 ⋅ч -1 объемной производительности, 67% содержания липидов и 0.Выход 234 г / г (5).
Анаэробный биореактор с пузырьковой колонкой.
M. thermoacetica выращивали в биореакторе со стеклянной барботажной колонкой с внутренним диаметром 4,5 см, высотой 80 см и общим рабочим объемом около 1 л (G. Finkenbeiner Inc.). Состав газа контролировали с помощью четырехканального регулятора массового расхода, регулирующего расход H 2 , CO, CO 2 и N 2 . Температуру биореактора поддерживали на уровне 60 ° C с помощью нагревательного одеяла и регулятора температуры.pH регулировали добавлением 5 н. гидроксида натрия или соляной кислоты, что определяли с помощью системы управления насосом Etatron DLX pH / ORP и погружного pH-электрода. Все цифровые контроллеры массового расхода, температуры и pH AALBORG были приобретены у Cole-Parmer. Подготовленную среду (за исключением цистеина) автоклавировали при 121 ° C в течение 25 минут, переносили в биореактор и продували бескислородным газом N 2 в течение ночи для удаления всех следов растворенного кислорода. После этого pH довели до 6.0, если не указано иное, и поток синтез-газа (описанный ниже) был инициирован и непрерывно барботировал через биореактор. К среде добавляли раствор цистеина (10 мл, 3% мас. / Мас.) Для удаления любого остаточного кислорода. Биореактор с пузырьковой колонкой инокулировали при 5% об. / Об. Культурой, выращенной в бутыле для сыворотки с использованием перечисленных выше сред.
Состав синтез-газа.
Первоначальные эксперименты в анаэробном реакторе проводились с составом исходного газа, который поддерживался постоянным на протяжении всего процесса ферментации.Клетки выращивали на смеси синтез-газа, подаваемой с общей скоростью потока газа 1000 sccm, и с составами CO / CO 2 (4/1) и H 2 / CO 2 (4/1). В последующих экспериментах, когда состав газа был изменен в середине ферментации, клетки сначала выращивали на CO / CO 2 (4/1) при 1000 sccm. После того, как клетки достигли стационарной фазы и выработка ацетата стабилизировалась, состав синтез-газа и скорость потока были отрегулированы, как описано ниже. В то же время половина среды в биореакторе была заменена свежей средой, и был инициирован поток через половолоконную мембрану для рециркуляции клеток обратно в биореактор.После замены среды рабочий объем барботажной колонки поддерживался постоянным на уровне 1 л.
Условия аэробного биореактора в резервуаре с перемешиванием.
Y. lipolytica выращивали в 2-литровом биореакторе с мешалкой (New Brunswick Scientific). Уровни pH и растворенного кислорода (DO) контролировали с помощью зонда pH и зонда DO (Mettler-Toledo Ingold Inc.). Исходная среда состояла из 30 г / л ацетата натрия (Macron Chemicals), 2,5 г / л дрожжевого экстракта (Difco Laboratories), 4.2 г / л дрожжевого азотного основания (без аминокислот и сульфата аммония; Amresco) и 2,4 г / л сульфата аммония (Macron Chemicals) (молярное отношение C / N 20). Заданные значения pH и DO составляли 7,3 и 20%, соответственно, и поддерживались каскадным контролем. PH регулировали путем подачи раствора уксусной кислоты. В течение первых 70 часов роста корм содержал 3% уксусной кислоты и 15 г / л сульфата аммония, чтобы обеспечить достаточное количество азота для образования нелипидной биомассы. Сырье содержало только 3% об. / Об. Уксусной кислоты до конца цикла.Дополнительный ацетат, необходимый для поддержания концентрации ацетата ~ 15 г / л в биореакторе, при необходимости подавали в виде раствора ацетата натрия (300 г / л). Модуль из полых волокон с размером пор 0,2 мкм и площадью поверхности 290 см. 2 (MiniKros Sample Plus Filter Module; Spectrum Laboratories) непрерывно использовали во время работы реактора для рециркуляции ячеек и удаления избыточного объема, закачанного в реактор. подача уксусной кислоты (20). Растворы уксусной кислоты готовили с ледяной уксусной кислотой (Acros Chemicals).Теоретический максимум накопления углерода определяется как образование липидов и нелипидов на ацетате (21, 22).
Интегрированная система биопроцессов.
Биореактор с барботажной колонкой (для M. thermoacetica ) и биореактор с мешалкой (для Y. lipolytica ) были объединены в процесс, схематически показанный на рис. 1. Условия эксперимента во время интегрированного цикла биопроцесса представлены в таблице 1. В этой системе газы поступают в барботажную колонну и превращаются в уксусную кислоту, которая, в свою очередь, используется в качестве сырья для реактора с мешалкой и превращается в липиды.Барботажная колонна сначала работала в периодическом режиме по отношению к жидкой фазе. Смесь газов CO / CO 2 подавали с составом 4: 1 и расходом 1000 куб.см. Через 94 часа состав газа был изменен на H 2 / CO 2 (2: 1), и скорость потока увеличилась до 1200 кубических сантиметров в секунду. В то же время 500 мл среды заменяли 500 мл свежей анаэробной среды с использованием половолоконной мембраны для удержания клеток в биореакторе (модуль MiniKros Sample Plus Filter Module; Spectrum Laboratories).Как только культура достигла стационарной фазы, через 185 ч, был инициирован поток жидкой среды, и биореактор с барботажной колонкой с M. thermoacetica был переключен на непрерывный режим работы со скоростью потока 0,5 мл / мин. Рециркуляция клеток также инициировалась одновременно с половолоконной мембраной. На протяжении всей операции pH поддерживали на уровне 6,0. Отработанные среды из половолоконной мембраны переносили в биореактор с мешалкой через стерильный контейнер. Биореактор с мешалкой (для Y.lipolytica ) инокулировали примерно через 33 часа после переключения на непрерывный режим, чтобы дать достаточно времени для подачи ~ 1000 мл ацетатсодержащей среды в биореактор. После инокуляции биореактор с мешалкой также работал в непрерывном режиме. Чтобы поддерживать постоянный рабочий объем в биореакторе, сточные воды, содержащие низкие концентрации уксусной кислоты, удаляли через половолоконную мембрану с размером пор 0,2 мкм и площадью поверхности 290 см. 2 (MiniKros Sample Plus Filter Module; Spectrum Laboratories ).Скорость потока жидкости увеличилась с 0,5 мл / мин до 1,5 мл / мин после инокуляции Y. lipolytica .
Анализ газов и жидкостей.
Расход газа измеряли с помощью пузырькового расходомера (Cole-Parmer). Состав газа анализировали с помощью двухканального микро-ГХ Agilent, оборудованного колонками PLOT U и Molecular Sieve, а также детекторами TCD (Agilent Technology). В качестве газа-носителя использовался аргон. OD измеряли при 600 нм с помощью кювет объемом 1 мл и спектрофотометра Ultrospec 2100 pro UV / Visible (General Electric).OD M. thermoacetica была пропорциональна DCW (соотношение ~ 0,45 г сухих элементов на литр на единицу OD 660 ) (23), значение подтверждено нашей лабораторией. Y. lipolytica Общую биомассу определяли гравиметрически с использованием фильтров из нитрата целлюлозы (Whatman). Фильтры сначала сушили при 60 ° C в течение 2 ч и предварительно взвешивали. В резервуар для выдержки, установленный на мембране фильтра, наливали 15 мл бульона. Применяли вакуум для протаскивания жидкости через мембрану.Фильтры сушили в течение 24 ч в сушильном шкафу при 60 ° C и повторно взвешивали. Ацетат и цитрат измеряли с помощью HPLC Waters Alliance 2695 с дифференциальным рефрактометром Waters 410 и колонкой Bio-Rad HPX-87H (Waters Corporation). Колонку элюировали при 35 ° C 14 мМ серной кислотой в качестве подвижной фазы со скоростью потока 0,6 мл / мин.
Экстракция и количественное определение липидов.
Общее количество липидов определяли количественно с использованием модифицированной версии протокола прямой переэтерификации, адаптированной из патента США 7932077 (24) и Griffiths et al.(25). Корреляцию между OD и биомассой клеток (0,3 г сухих клеток на литр на единицу OD 600 ) использовали для определения объема клеточной культуры. Объем клеточной культуры был выбран таким, чтобы каждый образец содержал ~ 1 мг клеточной биомассы. После центрифугирования и удаления супернатанта осадок клеток суспендировали в 100 мкл гексана, содержащего внутренний стандарт глицерилтригептадеканоат (триацилглицерид C17). Затем к смеси добавляли 500 мкл 0,5 н. Метоксида натрия и суспензию клеток встряхивали при комнатной температуре в течение 60 мин.Затем добавляли 40 мкл 98% (мас. / Мас.) Серной кислоты с последующим добавлением 500 мкл гексана. Всю эту смесь встряхивали в течение 30 мин при комнатной температуре для экстракции метиловых эфиров жирных кислот (FAME) в гексановую фазу. Наконец, смесь центрифугировали при 8000 об / мин (орбитальный шейкер Thermo Scientific MaxQ 4000 с орбитой 1,9 см) и верхний гексановый слой переносили во флаконы для анализа с помощью газовой хроматографии (ГХ). ГХ-анализ МЭЖК выполняли с использованием прибора Bruker 450-GC, оборудованного пламенно-ионизационным детектором и капиллярной колонкой HP-INNOWAX (30 м × 0.25 мм) и те же условия печи использовались, как обсуждалось у Tai и Stephanopoulos (2). Концентрации FAME были рассчитаны по коммерческим стандартам и нормализованы по внутреннему стандарту (метил C17) в контрольной пробирке без клеток. Общее содержание липидов рассчитывали как сумму общего содержания жирных метиловых эфиров для пяти FAME: метилпальмитата (C16: 0), метилпальмитолеата (C16: 1), метилстеарата (C18: 0), метилолеата (C18: 1), и метиллинолеат (C18: 2).
Анализ гидрогеназы.
Гидрогеназную активность оценивали путем мониторинга восстановления бензилвиологена проницаемыми клетками в запечатанной кювете (26). Раствор акцептора электронов (EA), состоящий из окисленного бензилвиологена и клеточного раствора (CS), взятого в результате ферментации, готовили в двух отдельных пробирках Hungate в анаэробной камере. Раствор EA содержал 0,3 мл 1 М калий-фосфатного буфера (pH 6), 0,4 мл 40 мМ бензилвиологендихлорида (BV) и 2,3 мл деионизированной воды. CS содержал 0.3 мл 1 M калий-фосфатного буфера (pH 6), 0,3 мл 0,5 M DTT, 0,3 мл клеточного бульона и 1,8 мл деионизированной воды. После подготовки обе пробирки вынули из анаэробной камеры и продули чистым газом H 2 со скоростью потока 50 см 3 / мин на водяной бане при 60 ° C в течение 5 мин. За одну минуту до окончания продувки в пробирку CS вводили 0,3 мл раствора Triton X-100 для проникновения через клеточную стенку и воздействия раствора на гидрогеназу. Чтобы начать анализ, 2 мл из пробирки с раствором EA и 0.67 мл из пробирки CS смешивали в герметичной анаэробной кювете, и восстановление BV ox до восстановленного BV red непрерывно отслеживали при 546 нм. Активность (U) рассчитывалась исходя из начального наклона с использованием коэффициента экстинкции 7,55 м 3 мкмоль -1 мкм -1 . Одна единица была определена как потребление 1 мкмоль H 2 в минуту. Удельную активность (Ед / мг) определяли делением активности на клеточную массу в анализе.Следует отметить, что определенная активность представляет собой общую ферментативную активность всех гидрогеназ, участвующих в поглощении водорода. Предыдущие исследования показали, что несколько различных ферментов гидрогеназы активны в ацетогене M. thermoacetica (27).
Благодарности
Мы благодарим доктора Викторию Бертис и доктора Питера Гиргуиса (Гарвардский университет) за их помощь. Это исследование было поддержано грантом ARPA-E программы Electrofuels (Award DE-AR0000059) и Программой геномных наук Министерства энергетики (Grant DE-SC0008744) (MIT: 692-6611).
Сноски
Вклад авторов: исследование, разработанное G.S. P.H., S.C. и H.L. проводили исследования; A.K., B.W., D.E. и G.S. проанализировали данные; и А.К. и Г.С. написали статью.
Авторы заявляют об отсутствии конфликта интересов.
Эта статья представляет собой прямое представление PNAS.
См. Комментарий на стр. 3717.
Эта статья содержит вспомогательную информацию на сайте www.pnas.org / lookup / suppl / doi: 10.1073 / pnas.1516867113 / — / DCSupplemental.


 Преимущества: полная энергонезависимость, небольшая стоимость. Минусы: огонь контактирует с воздухом в помещении, некоторые жалуются на запах газа при сжигании пропана посредством атмосферной горелки.
Преимущества: полная энергонезависимость, небольшая стоимость. Минусы: огонь контактирует с воздухом в помещении, некоторые жалуются на запах газа при сжигании пропана посредством атмосферной горелки.

 Присутствуют минимальные функции: механический блок управления, опция переключения режимов «зима-лето».
Присутствуют минимальные функции: механический блок управления, опция переключения режимов «зима-лето».
